锂离子电池电解液SEI成膜添加剂的研究进展
引言
锂离子电池因其具有高电压、高容量、无记忆效应、寿命长等显著优点,目前已被广泛用于计算机、移动电话、电子手表和其他便携性电子设备中,未来在智能电网、先进储能、智能建筑等领域也会有广阔的发展前景[1-5]。2021年4月国际能源署的技术报告——《全球电动汽车展望》报道,经过十年的快速增长,到2020年底,全球公路上的电动汽车数量达到1000万辆,比2019年增长43%,市场份额达到1%;2020年汽车锂离子电池产量为160 GWh,比2019年增长33%;2020年,电动汽车在全球节省了超过5000万吨二氧化碳当量的温室气体排放量,这些节省主要来自中国的电动两轮/三轮车[6]。随着锂离子电池应用范围不断扩展,人们对锂离子电池也提出了更高的要求:具有更高的能量密度和循环寿命,更高的安全性,更宽的服役温度范围,更低的自放电速率和更低的原材料成本。
锂离子电池主要由正极材料、负极材料、电解液和隔膜四大关键部分组成。锂离子电池放电过程为:锂离子从阳极脱出,穿过SEI膜进入电解液中,在电解液中通过扩散传输到阴极表面,最后通过嵌入阴极材料实现嵌锂过程,实现放电,充电与此过程相反。锂离子从阳极到阴极过程中的顺利传输是关键,因此电解液作为运输锂离子的载体成为影响锂离子电池性能的关键。电解液主要由溶剂、锂盐和添加剂组成。其中溶剂主要作为运输锂离子的载体,对电解质盐进行溶剂化作用,保证锂离子的传输,常见的是羧酸酯和碳酸酯溶剂;锂盐则是锂离子的提供者,影响电池的倍率及循环性能,目前市场上的锂盐主要选用LiPF6;添加剂是最经济、高效提升电池性能的方法。因为其添加量较少(通常浓度不超过5%),几乎不增加电池的成本, 但却能增加电解液的功能, 显著提高电池的性能,是近年来锂离子电池电解液领域研究的核心方向[7-9]。与其他行业一样,电解液生产的既定基础设施使现状难以发生任何大规模变动,除非有重大突破出现。因此,如果可以通过在电解液中加入少量成分而不更换其骨架成分来实现某些电池性能的改善,则将更加经济和方便。有关锂离子电池电解液添加剂的研究最早可追溯到Peled等[10]探索的一种方法,该实验小组证明了溶剂化电子与电解质组分和杂质反应的速率常数(ke)与SEI膜的形成电压和SEI膜的组成密切相关。因此,ke可作为选择电解质溶剂和盐的工具。根据该模型,理想电解液的配方应符合ke >109 L/(mol·s)。该模型在概念上形成了电解质添加剂后期开发的理论基础[1]。添加剂根据使用功能的不同,可以分为如下几类:成膜添加剂、阻燃添加剂、过充保护添加剂和其他多功能添加剂等。其中成膜添加剂主要是对SEI膜的化学性质和表面结构进行优化,良好的SEI膜对提高锂离子电池的循环寿命有重要的作用。本文梳理最近几年锂离子电池电解液SEI成膜添加剂的研究进展,进行总结,为将来SEI成膜添加剂的研发提供了借鉴和参考。
1 SEI概述
有关SEI膜的研究最早可以追溯到20世纪70年代前后,科研人员发现在锂金属电池中,锂金属在许多非水溶剂中是稳定的。研究人员认为电解液对锂表面的钝化是这种意外稳定性的根源,因为这些有机溶剂的还原电位远远高于锂[11]。Peled[12]于20世纪70年代末提出了SEI模型,该模型表明碱金属和碱土金属在SEI-非水电池体系中的沉积-溶解机制与在水相或类水相体系中的沉积-溶解机制是完全不同的。由于该钝化膜为离子导体但却是电子绝缘体,其导电性方面类似于电解质一样,因此将其命名为“固体电解质界面”。Dahn等[13]在发表的报告中也沿用了Peled提出的模型来描述金属锂的钝化,将碳质阳极上的这种表面膜也命名为“固体电解质界面”。该词已成为锂离子电池相关出版物中最常见的关键词。
直到今天,SEI仍然被认为是“锂离子电池中最重要但了解最少的”,这是因为形成它的电化学反应的复杂性以及对其物理性质的直接测量方法的不足所导致的[14-15]。SEI膜的化学成分被认为与电解液的成分密切相关,当电解液用锂盐为LiPF6、LiBF4、LiAsF6 等含氟锂盐时,SEI 膜的主要成分是LiF[16];当溶剂为碳酸乙烯酯 (EC)、碳酸丙烯酯(PC)、碳酸二甲酯(DMC)等碳酸酯类有机溶剂时,SEI 膜的主要成分是 Li2CO3和碳酸烷基锂[17];当溶剂为醚类有机溶剂时,SEI 膜的主要成分是烷基氧锂和烷基碳酸锂等[18]。Wang等[19]认为SEI膜在靠近电极界面内层以稳定的Li2CO3、Li2O、LiF等无机物为主,界面外层以ROLi、ROCO2Li等有机物为主,在SEI/电解液界面附近,多孔且可渗透Li+和溶剂分子。其内层结构致密紧实,外层结构疏松多孔。
虽然在最近十几年的时间里科研人员对SEI膜的化学组成、表面结构、形成机理和电化学性能做了一系列的研究,但是目前对SEI膜的性质仍然有很多疑惑未被很好解释,一方面是因为SEI膜自身结构十分复杂,影响其化学成分和表面结构的因素包括电解液锂盐、溶剂、温度和电流密度等,而且缺少先进的测试手段对其进行深入分析[20-22];另一方面是由于SEI膜对空气是比较敏感的,接触微量的空气就有可能改变其原有的组分和表面结构[23-25]。当前用来表征SEI膜的测试手段主要包括原子力显微镜(AFM)、扫描电子显微镜(SEM)、X射线光电子能谱(XPS)、傅里叶红外光谱仪(FTIR)、透射电子显微镜(TEM)、拉曼光谱(Raman)、热重分析仪(TGA)、差示扫描量热仪(DSC)等[26]。
研究人员经过反复实验确立了一个半经验规则,该规则通过最低未占用分子轨道(LUMO)的能级来判断某种化合物在阳极上是否被还原。该规则的基础是假设LUMO能量水平较低的分子应该是更好的电子接受者,因此,在阳极的负电荷表面上反应更灵敏[3]。显然,所有脂肪族环碳酸酯的LUMO 水平几乎相同,而具有芳香键、双键或卤素原子替代的结构修饰会导致 LUMO 水平大幅下降[27]。LUMO 能量水平与这些添加剂的还原电位之间存在一定的关系。
2 SEI成膜添加剂
碳负极形成的SEI膜对于锂离子电池的循环寿命、放电倍率和低温性能有重要影响。SEI成膜添加剂能够优先在电极表面发生氧化还原反应,促进生成致密、稳定的SEI膜,因此选择合适的SEI成膜添加剂是十分有必要的。成膜添加剂主要包括不饱和酯类添加剂、含硫添加剂、锂盐类添加剂、无机化合物类添加剂和其他添加剂等,本文重点阐述近五年成膜添加剂的研究成果。
2.1 不饱和酯类添加剂
酯类添加剂主要有VC、FEC、VEC、CC、AEC、VA等,其分子结构如图1所示。VC应该是比较经典的成膜添加剂,VC的反应活性来自其可聚合乙烯基的功能性和高应变结构,这是由环上的sp2杂化碳原子引起的[28]。
图1

图1 常见不饱和酯类添加剂的分子结构
Fig.1 Molecular structure of common unsaturated ester additives
VC的成膜机理是能够优先于电解液发生还原,因此能够优先形成SEI膜。Lin等[29]发现1%的VC在电解液中可以在较高电位下促进初始SEI的形成,还抑制了EC的还原,如图2所示。VC首先发生还原反应,并在HOPG基面上形成许多颗粒,之后的EC还原有助于在未覆盖的HOPG表面上形成薄层。Guo等[30]对EC/PC为共溶剂、VC为添加剂的离子液体基混合电解质体系进行了评估。结果表明VC的存在可以在电极界面上形成SEI,阻止EC的还原分解,SEI同时也促进了Li+能够有效插入石墨中。
图2
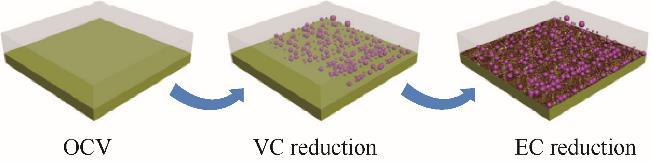
图2 在含有1%VC的1.0 mol/L LiPF6/EC/DMC中,HOPG电极上不同表面演化阶段的示意图[29]
Fig.2 The schematic of different surface evolution stage on HOPG electrode in 1.0 mol/L LiPF6/EC/DMC with 1% VC[29]
Petibon等[31]探究了VC对1 mol/L LiPF6 EC∶EMC[3∶7 (质量比)]中LiCoO2/石墨电极电池的影响。电化学阻抗谱(EIS)测量结果表明,VC的所有浓度对正极都有影响,当浓度高于1%时对负极有影响。Haruna等[32]认为在阳极处还原分解的VC具有上限,而在阴极处氧化分解的VC很大程度上取决于初始VC浓度。Pritzl等[33]利用OEM和EIS以及微参比电极来分析VC的氧化稳定性及其对阳极和阴极界面电阻的影响。研究发现VC的添加量与钝化膜的形成顺序有关,当向石墨/LNMO电池中添加少量VC[0.09%(质量分数)]时,它将优先在石墨阳极处还原。当电解液中存在较高浓度的VC[0.17%~2% (质量分数)]时,VC将在阴极氧化导致阴极阻抗变大。如图3所示,VC不仅有助于在石墨负极形成优异的SEI膜,而且可以在正极形成性能相当的CEI膜[34]。
图3

图3 向电解液中添加VC时表面保护层形成过程的示意图[34]
Fig.3 Schematic illustrations of the postulated formation process of surface protective layer when VC was added to the electrolyte[34]
由于VC添加剂有优异的成膜能力,因此能够提高电池的库仑效率和充电容量保持率。Deshpande等[35]研究了VC添加剂在石墨/NMC333电池中的作用,研究证明添加VC可以提高速率性能,并且随着VC的增加,副反应的发生率降低。Brown等[36]也证明了向电解液中添加VC可提高容量保持率和效率。Lim等[37]通过溶剂交换法成功制备了VC填充的微胶囊,该方法允许VC在高温下通过微胶囊壳壁扩散,如图4所示。相比之下,与直接向电解液中添加VC相比,通过微胶囊扩散的VC的时间释放在5 C下增加了2.5倍的放电容量。该方法为添加剂的设计提供了一个新的思考方向。
图4
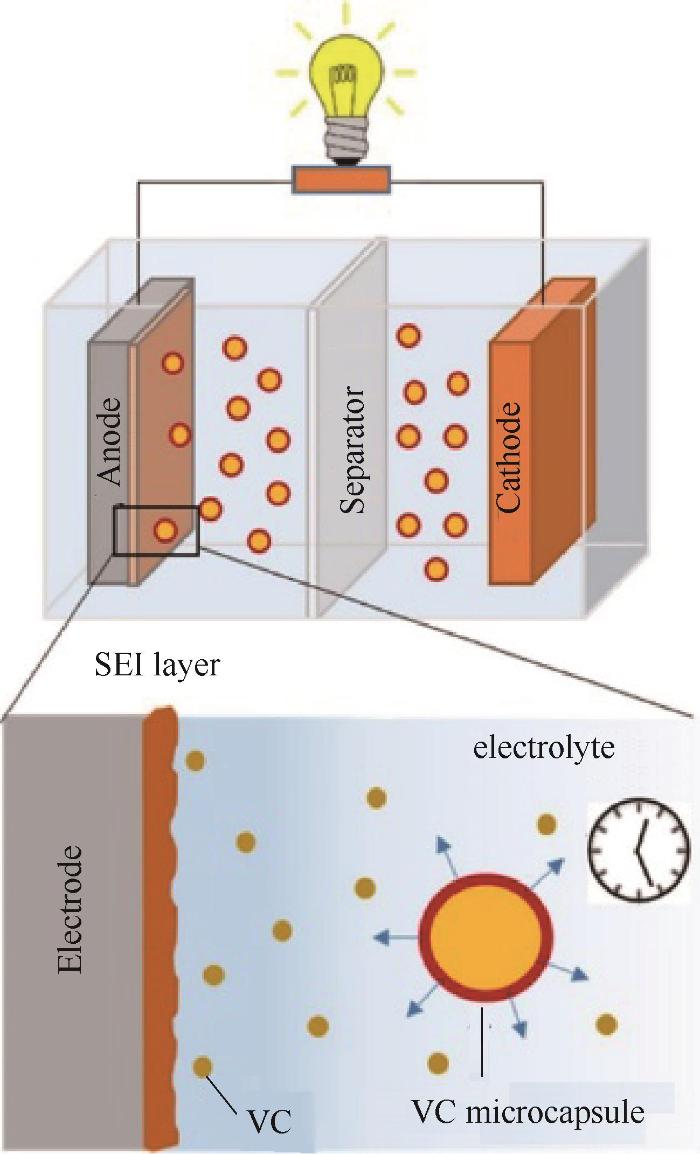
图4 锂离子电池中基于微胶囊的VC添加剂释放示意图[37]
Fig.4 Schematic of microcapsule-based release of VC additives in a Li-ion battery[37]
总地来说,VC 作为经典的电解液成膜添加剂,在较低电压下5%以内的 VC 几乎对绝大多数电池体系的电化学性能有改善作用[38]。但是VC添加剂对锂离子电池阴极的热性能和安全特性会产生负面影响[39]。由于VC在高温条件下电化学性能较差,因此在实际中往往需要和其他的功能添加剂一起使用。VC和1,3-PS的共同使用则可以大大延长电池的循环寿命,并抑制其在高温下的膨胀行为,二者的协同作用源于乙烯基和砜官能团的结合,以便提供具有交联保护网络的钝化膜[40-41]。
FEC是EC的单F原子取代产物,由于F具有很强的电负性和弱极性,导致该添加剂的凝固点较低、氧化稳定性较高以及提高了电极/电解液界面的兼容性,因此提高了电池的低温性能、抗氧化性能和电极润湿性[42-43]。FEC添加剂可以形成富LiF的固体电解质界面,其诱导形成的SEI层致密稳定,有利于获得均匀的Li沉积形态[44-47]。LiF可能促使锂离子分布更均匀,并抑制无序锂枝晶的出现。近些年含氟或氟化物电解液被重点关注,也说明LiF是一种特别有利的SEI组分。FEC添加剂的优先还原被认为有利于阳极表面的早期钝化,并促进SEI成分的改善[48]。Yang等[49]研究发现Li+在LiF中具有较低的扩散势垒,通过引入FEC可以增加表面SEI中LiF的含量,从而促进界面处的锂离子扩散。研究证明添加FEC的电极的循环性能和速率性能得到提高[50]。Liu等[51]研究发现在3.0~4.4 V的电压范围内,电池在含5%FEC的电解液中表现出更好的循环性能,且FEC有助于形成稳定的SEI界面。Zhang等[52]研究发现使用FEC添加剂之后能够在负极形成致密的SEI膜,这种均匀且无枝晶的形态使得Li|Cu半电池在100个循环内的库仑效率提高了98%。Meng等[53]研究了一系列添加剂后发现以FEC为添加剂的电解质锂离子电池在循环过程中的容量保持率最高。
Hou等[54]通过经典分子动力学、傅里叶变换红外光谱和量子化学计算,证实了FEC作为电解质添加剂可以显著改变溶剂化结构和SEI的形成过程,如图5所示。有限数量的FEC的加入可以促进离子对结合,触发阳极钝化的早期发生,促进LiF的形成,并可能通过形成亚稳中间体促进SEI中的聚合。然而,单独使用FEC添加剂可能会导致锂离子电池的循环性能下降[55]。Kitz等[56]研究发现FEC分解产物会阻碍通过SEI的电荷传输,从而显著增加整体阳极阻抗。Arnot等[57]研究发现,有FEC的电池比没有FEC的电池显示出更高的平均寄生反应焓,从而降低了发生副反应的概率,这是因为平均寄生反应焓随温度升高而降低。近年来,可持续SEI被提出作为一种新的设计原则,以应对来自实际条件的挑战。Zhang等[58]首次在实际条件下研究了由FEC作为共溶剂生成的F-SEI和由LiNO3缓释形成的N-SEI的可持续性,在此基础上,提出了F-SEI和N-SEI的合理组合,以在碳酸盐电解质中构建可持续的氟化氮化SEI(FN-SEI)。除常见的石墨阳极,FEC在其他阳极也能够形成稳定的SEI膜,FEC的存在有助于产生富LiF的SEI,可有效防止连续电解质分解[59-60]。
图5

图5 在EC和FEC电解液形成过程中计算的微分电容图[54]
Fig.5 The calculated capacity plots during the formation step of EC and FEC electrolyte[54]
综上所述,使用单一添加剂很难同时满足所有预期性能。因此,多元添加剂是未来的发展战略。最常见的成膜添加剂组合是VC和FEC,二者协同可以抑制溶剂的连续还原,该组合常见于对硅阳极的SEI膜进行优化[61-62]。Hu等[63]制备了100个晶体取向硅微柱阵列平台用于研究FEC、VEC、ES和VC作为添加剂的性能。结果表明,无机锂盐能够形成更平滑、更平坦的膜,而较高含量的有机锂盐会形成更粗糙的电极表面,如图6所示。FEC和VC电极表面的聚VC成分允许硅柱在保持完整的同时容纳更大的体积膨胀。SEI膜中的聚锂盐组分可以进一步降低SEI膜的rSEI阻抗,提高锂离子的扩散系数。这种硅微柱平台和分析方法能够深入分析添加剂的综合性能,为电解液添加剂的性能分析提供了一种标准有效的测试方法,并为新型电解液添加剂的开发提供了指导。
图6

图6 五种电解液中10次充放电循环后硅微柱阵列电极的SEM图像[(a)~(e)]; 晶体Si〈100〉晶面原子分布示意图(f) [63]
Fig.6 SEM images of Si micropillar array electrodes after 10 charge/discharge cycles in five electrolytes[(a)~(e)]; Schematic diagram of the atomic distribution of crystal Si〈100〉 crystal plane (f) [63]
其他的酯类添加剂还有VEC、CC、AEC、VA等,它们都对SEI膜有稳定作用。Xu[64]通过研究发现,含有VEC的电解液的SEI膜在锂离子插入过程中更稳定,并且能够灵活地适应石墨材料的体积变化,从而使锂离子的嵌入/脱嵌具有更好的可逆性。除此之外,研究人员还发现VEC可以改善电池的高电压稳定性以及容量保持率[65-66]。
2.2 含硫添加剂
含硫添加剂主要指磺酸内酯和硫酸酯等添加剂,硫化物和亚砜极不稳定, 因此应用较少, 而砜类物质氧化稳定性较强[38]。其中具有代表性的成膜添加剂主要包括PS、ES、DES、PES、DMS、VES、DTD、TMS、FPS、SPA等,其常见分子结构如图7所示。
图7
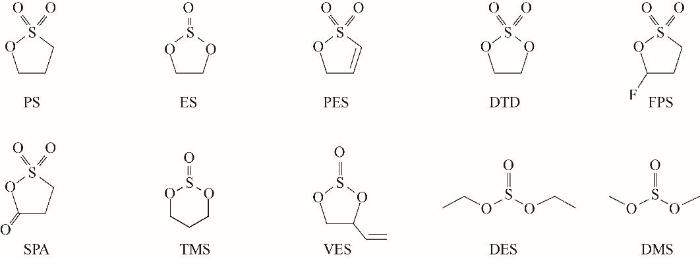
图7 常见含硫成膜添加剂的分子结构
Fig.7 Molecular structure of common sulfur containing additives
PS的研究最早是由于其能够改善SEI膜与石墨负极的兼容性[67-68]。Park等[69]发现在PC基电解液中添加PS可以显著抑制石墨电极对溶剂的分解,从而改善电池的电化学性能。这从侧面表明了PS对SEI膜的形成有一定的影响作用,而Yoon等[70]发现PS在硅氧化物电极下形成的SEI膜具有比较小的电阻,使得电池具有低不可逆容量和良好的循环性能。除此以外,PS还具有提高锂离子电池循环性能的作用,这可以归因于PS对SEI膜进行了修饰,从而有效防止阳极和阴极结构破坏,并抑制电解质分解[71]。PS对电池容量保持率的提高则源于其参与了钝化层的形成,从而防止了金属从阴极材料中溶解[72-73]。
随着计算材料学的飞速发展,利用计算机能够快速筛选出合适的添加剂,从而避免了“尝试法”的周期长、效率低的科研过程。Lin等[74]应用DFT研究了PS在锂离子电池阳极表面附近形成SEI膜的还原反应,如图8所示。在溶剂状态下,PS的还原速度快于EC,减少了C2H4的生成,减轻了电池的膨胀现象。PS及其初始产物的还原能力较高,而其后续产物的还原能力较低,这意味着还原反应可以终止,这将是还原型添加剂形成有效SEI膜的关键特性。Xu等[75]研究发现含有2%PS的电池比不添加PS的电池具有更好的容量保持能力,这很好地印证了PS在负极的优异的成膜能力。此外,Jung等[76]发现氟取代的PS产物——FPS具有高阳极稳定性、优异的循环性和良好的热稳定性,可以较好地扩展当前锂离子电池的性能边界。
图8
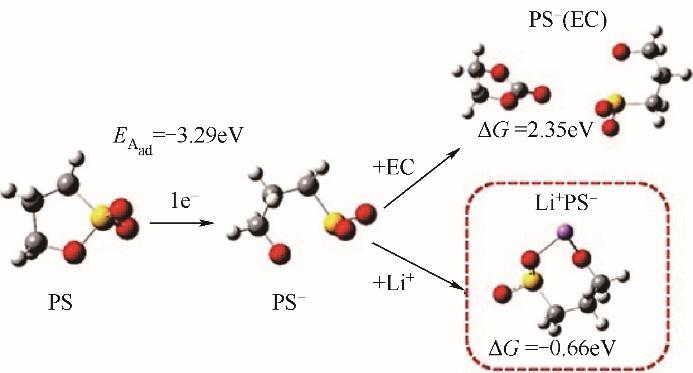
图8 PS的主要还原过程[74]
Fig.8 Main reduction process of PS[74]
PES比起PS多一个不饱和度,选择PES替代PS作为SEI形成添加剂的主要驱动力是其更强的电化学还原倾向,其由与磺酸盐相邻的碳碳双键赋予其更强的电化学还原趋势。Li等[77]首次报道了有关PES作为成膜添加剂的研究。PES可以比PS先还原,使用PES作为添加剂的PC基电解质的电池具有更小的初始容量损失和更好的循环稳定性。随后研究人员使用理论计算和实验验证了PES添加剂在锂离子电池中的成膜机理和PES还原分解的几种自发途径[78-79]。后来的研究也表明了PES对石墨阳极的SEI膜稳定性提升有很大作用,并且电池的容量保持率得到显著提高[80-81]。
ES也具有相当优异的SEI膜形成能力,其形成保护性SEI的主要产物为Li2SO3、CH3CH(OSO2Li)等含硫有机物[82]。Bhatt[83]采用DFT理论研究了VC、VEC、VES和ES等电解质添加剂在PC基锂离子电池电解液中对石墨阳极上SEI形成的影响。数据表明,某些添加剂(尤其是亚硫酸酯)在PC基电解液中对石墨碳基锂离子电池阳极的SEI膜形成和稳定循环起到了支持作用,而不会导致阳极结构剥落或退化。Li等[84]研究发现添加ES可在一定阶段抑制无机化合物的形成,从而改变石墨阳极表面SEI涂层的组成,能够显著降低SEI层和石墨阳极电解质界面的电阻。和PES相比,ES能在更高的电压下开始形成SEI,具有更高的电池稳定性,SEI层的表面看起来更致密光滑且更厚[85]。ES具有良好的成膜能力,其对锂离子电池低温性能的改善也有很大的作用,也被经常用作全固态锂离子电池的成膜添加剂[86-87]。
DTD能够在溶剂之前被还原,但如果添加量过少则成膜效果大大削弱,添加DTD的石墨负极可以形成一层光滑的SEI膜,有效降低了SEI阻抗[88-89]。Madec等[90]发现在PC中使用10%(质量)的DTD能够在石墨上形成有效且稳定的SEI,且DTD的分解发生在PC共交联之前,因此可以防止石墨剥落。Zhang等[91]也研究发现,DTD通过在电极表面的还原分解反应参与成膜过程,能够生成均匀致密的SEI膜。DTD作为单一添加剂与VC的性能相当,但当DTD与其他添加剂(PES、VC)共同使用时往往能得到更好的成膜效果[92]。为了更好地了解背后的原因,Janssen等[93]提出了PES/DTD共混物协同的假设:PES在负极上还原形成亲核试剂,与亲电的DTD反应,产生钝化层,从而抑制了DTD或溶剂的直接还原。Zhang等[94]通过DFT计算表明,DTD具有相对较低的最低未占据分子轨道(LUMO)能量,在石墨阳极上更容易还原。SEM图像显示,添加1%DTD后,石墨电极表面形成SEI膜,使电极表面更加光滑和均匀。Nelson等[95]研究了DTD、PS、PES、SPA和EC作为成膜添加剂的作用,如表1所示。DFT计算发现所有添加剂都具有比EC更低的LUMO能级和较高的电子亲和力,表明它们有利于还原反应的发生。更进一步讲,这是因为双键或羰基的引入显著增强了还原能力。引入双键或羰基会使得化学硬度变低,硬度较低的分子在其还原形式下会更稳定,这能够以更慢、更可控的方式创建SEI层。此外,DTD不但有良好的成膜能力,还可以显著改善高压电极的循环性能和低温性能。除了石墨负极,DTD还具有与硅电极的高相容性。DTD的衍生物也具有与DTD相似的成膜效果,如D-DTD。与用DTD添加剂在电解液中循环的电极相比,D-DTD添加剂促进了更薄的界面层,该界面层更完整、更均匀。
表1 偶极矩、HOMO和LUMO能级能量、电离势(IP)、电子亲和性(EA)、化学硬度(η)以及与锂离子相互作用的Gibbs自由能(ΔG)[95]
Table 1
| 参数 | DTD | PS | SPA | PES | EC |
|---|---|---|---|---|---|
| dipole/D(1D = 3.33563 ×10-30 C·m) | 7.99 | 8.45 | 7.40 | 8.64 | 7.33 |
| HOMO/eV | -10.77 | -10.33 | -10.67 | -9.89 | -10.62 |
| LOMO/eV | 0.04 | 0.03 | -0.10 | -0.27 | 0.06 |
| IP/eV | 9.6 | 9.02 | 9.21 | 8.78 | 9.55 |
| EA/eV | 0.66 | 0.69 | 1.08 | 1.45 | 0.65 |
| η/eV | 4.48 | 4.16 | 4.06 | 3.67 | 4.36 |
| ΔG(Li+)(neutral)/(kJ/mol) | 3.76 | 0.85 | 3.70 | 1.20 | 0.45 |
| ΔG(Li+)(anion)/(kJ/mol) | -19.56 | -15.72 | -24.73 | -18.42 | -41.54 |
其他的含硫添加剂如TMS、VES、DES、DMS等也对SEI膜的修饰起到了重要的作用,在锂离子电池中引入TMS添加剂被认为是去除电解液中HF的有效方法,这可以大大减缓SEI膜的腐蚀程度,降低电极/电解质界面的损坏,有益于理想的SEI膜的形成[96]。VES由于其较低的LUMO能级倾向于在EC或PC之前被还原,因此有助于电极的成膜能力。DES具有良好的成膜能力,因此添加DES的锂离子电池的容量保持率和低温性能表现也十分优异[97]。Li等[98]研究了DES作为NCM811/石墨电池添加剂的影响,电化学测试和光谱表征表明,这种功能化的DES电解质添加剂能够很好地调节阳极和阴极界面,具有更稳定的膜和更小的阻抗,从而促进界面Li+的嵌入和脱嵌。此外,界面膜还可以抑制过渡金属元素镍从阴极的溶解,保护NCM811材料的结构稳定性。含有DES添加剂的电解液在NCM811/石墨电池的应用中显示出良好的前景。
总的来说,含硫添加剂的特点主要是硫的价态较多,分解产物与分解路径不一,尚无普遍的还原机理。因此含硫添加剂诱导形成的SEI膜化学组成和界面结构也会有不同的结果,这可能会导致意料之外的性能出现。如何设计含硫添加剂,使其副反应和气体尽量减少也是一个值得深入研究的方向。目前最常见的组合方式并非单一使用含硫添加剂,而是与其他类型的成膜添加剂一起构成复合添加剂使用,达到取长补短的目的。探索含硫添加剂与其他成膜添加剂的协同规律能够更高效开发新型成膜添加剂,DFT结合其他理论的应用能够提高筛选的效率。
2.3 锂盐类添加剂
当前在锂离子电池中使用最广泛仍然是LiPF6。其他锂盐在某一性能上可能比LiPF6的性能更好,但这些锂盐都不能像LiPF6那样同时满足这些多方面的要求[1]。LiPF6对痕量水敏感和热稳定性差也是当前主要困扰锂离子电池继续进步的原因,为了缓解这一问题,科研人员试图通过制备新型锂盐来解决这一问题。
当前新型锂盐开发的基本原则是改变锂盐中的阴离子种类,其中以配合物阴离子最为有效。这些新型锂盐主要包括LiBOB、LiODFB、LiTFOP、LiPO2F2、LiTFSI、LiFSI、LiBODFP等,其常见的分子结构如图9所示。但这些新型锂盐都并非完美,因此并不能完全替代LiPF6,所以大多数都只能当作添加剂来使用。
图9

图9 常见锂盐添加剂的分子结构
Fig.9 Molecular structure of common lithium salt additives
双草酸硼酸锂(LiBOB)最早由Xu等[99]发现,并在之后得到了广泛的研究。LiBOB在电池循环过程中会稳定石墨负极,可以抑制电解液持续发生的氧化分解,具有很好的成膜性能和热稳定性[100-101]。Lian等[102]发现LiBOB在第一次充电期间会在阴极表面发生氧化,形成了含有少量LiF和大量有机物的SEI层,降低了界面极化,从而减轻了富锂阴极的电压衰减现象。姜雪等[103]通过研究发现,LiBOB能够提高Li1.15Ni0.68Mn1.32O4电极的循环性能的原因是LiBOB能够在其表面形成稳定的SEI膜,从而抑制了Mn的溶解,保证了电极材料结构的稳定。Kranz等[104]的研究表明Li+在SEI的孔隙中传输,对于含LiBOB电解液中形成的SEI,孔隙内的液相Li+传输比穿过SEI固相的Li+传输更快。这主要是因为LiBOB的加入使得SEI膜致密的内层变得更厚,孔隙通道更长,导致传输速率加快。除了对石墨负极有良好的成膜能力外,LiBOB对正极材料也具有良好的成膜能力。Ha等[105]发现LiBOB能够抑制电解液的氧化分解并稳定阴极的SEI,具有良好的成膜效果。Xiao等[106]研究发现LiBOB和活性氧自由基之间的反应会形成致密的阴极电解质界面膜,这有助于抑制富锂层状氧化物正极材料的容量和电压衰减。综上所述,LiBOB作为成膜添加剂,对正极和负极材料的成膜能力都起到了较大的提高作用,使得电池的循环性能、离子传输速度得到了改善,降低了容量衰减现象。LiBOB缺点是溶解度较低,形成的SEI阻抗较大导致高倍率放电性能下降。因此未来还需要对LiBOB的化学结构进行优化,寻找合适的低黏度的电解液配比来提高LiBOB的溶解度。
与LiBOB相比,LiODFB可以看作是LiBF4和LiBOB各自化学结构的一半而形成的新型锂盐,因此兼具了LiBF4和LiBOB各自的优点。LiODFB具有良好的成膜能力和优异的低温性能,能形成更稳定的钝化膜,具有更低的界面阻抗[107]。Bhatt等[108]利用DFT计算了PC基锂离子电池电解液中FEC、LiBOB和LiODFB作为电解液添加剂的反应性、还原性和作用,根据其各自的LUMO能级和HOMO-LUMO间隙能遵循LiBOB>LiDFOB>FEC。数据证明了LiBOB和LiDFOB在PC基电解液中对SEI膜形成和石墨阳极稳定循环有很好的支持作用,而不会使阳极结构退化。Liu等[109]对添加和不添加LiODFB的NMC111-石墨全电池进行了电化学测试。EIS表明,含LiODFB的全电池的界面阻抗比标准电池低得多,如图10所示。DFT计算表明,由于其较高的环应变,LiODFB在石墨表面能够以比EC更高的还原电位生成一层薄且有弹性的SEI膜,保护石墨免受Mn2+的影响,从而改善了NMC石墨基电池的电化学性能。
图10

图10 基于标准和改良电解液的全电池EIS[109]
Fig.10 EIS of full-cells based on standard and modified electrolyte[109]
除了单独使用LiODFB作为成膜添加剂,LiODFB还能够与其他成膜添加剂起到协同作用提供更好的性能。Gao等[110]使用LiODFB和LiTFSI作为锂盐的二元电解液,经测试发现半电池的放电容量和库仑效率有了巨大的提升,这一显著的改进归因于ODFB-和TFSI-阴离子的联合氧化分解,从而在电极上形成完美的SEI膜。除了具有优异的成膜能力,LiODFB还具有良好的低温性能、热稳定性[111]。Zhao等[112]研究了不同摩尔比的LiODFB和LiBF4混合盐的电化学行为,该电解液不仅具有优良的成膜特性,而且在低温下可以形成具有低阻抗的界面膜,如图11所示。Gu等[113]以LiODFB为添加剂,制备了一种新型安全电解液。这种高安全性电解液有助于石墨/LiNi0.5Co0.2Mn0.3O2全电池获得卓越的电化学性能,使用该电解液的电池在-40℃下可提供约90 mAh/g的放电容量。
图11

图11 不同电解质体系的离子电导率与温度的关系[112]
Fig.11 Dependence of ionic conductivity on temperature for different electrolyte systems[112]
综上所述,LiODFB在用于锂离子电池电解质时,结合了LiBOB的成膜性能和LiBF4盐的低温性能。因此使用LiODFB作为添加剂的锂离子电池的SEI成膜效果显著增强,并由此提高了循环性能和放电容量。然而,和LiPF6或LiTFSI等锂盐相比,LiODFB在离子液体中的溶解性较差,因此需要为LiODFB寻找合适的溶剂体系来提高溶解度。
LiPO2F2是近年电解液添加剂研究的热点之一。LiPO2F2最早被作为 LiPF6 制备过程中的副产物而未被重视。近年来研究人员发现添加 LiPO2F2 后正负极材料的SEI阻抗显著降低,能够保证电解液的电化学稳定性,从而显著提高电池的循环寿命,高低温、倍率性能等[114]。Kim等[115]研究表明,LiPO2F2能够修饰SEI膜,加快了石墨负极/电解液界面电荷的传输速度,确保了良好的速率性能。Yang等[116]通过DFT计算和测试结果表明,LiPO2F2能够在石墨阳极和LiCoO2阴极表面沉积,抑制了阴极材料的分解,有力地保护了石墨阳极。Hong等[117]研究发现LiPO2F2添加剂在阴极表面能够生成更均匀、更稳定且电阻更低的钝化膜。该钝化膜不仅可以抑制电解液的后续分解,还防止过渡金属离子从NCM523颗粒中溶解,从而提高NCM523/石墨电池的循环稳定性和放电能力。Zhao等[118]通过深入的实验表征和理论计算表明,LiPO2F2在阴极表面形成了一层新的稳定SEI膜,其成分为LiP2F2、LiF等,显著降低了电极的电荷转移阻抗,如表2所示。
表2 无添加剂和1.0%LiPO2F2样品的EIS拟合结果[118]
Table 2
| Sample | After the 1st cycle | After the 50th cycle | After the 150th cycle | |||
|---|---|---|---|---|---|---|
| rSEI/Ω | rct/Ω | rSEI/Ω | rct/Ω | rSEI/Ω | rct/Ω | |
| no additive | 14.4 | 8.6 | 1.7 | 30.2 | 4.6 | 162.5 |
| 1% LiPO2F2 | 10.3 | 5.7 | 1.9 | 3.1 | 2.8 | 3.8 |
Liu等[119]研究了LiPO2F2在LNMO阴极上的成膜机理,随着CEI薄膜的生长,LiPO2F2优先分解产物可以逐渐阻止电解液与阴极的接触,从而减少电解质的分解,如图12所示。直到生长的CEI膜足够致密,能够有效隔离电解液和阴极,由含有LiPO2F2的电解液形成的CEI膜更有利于Li+的传输,最终让高压锂离子电池拥有了优异的电化学性能。
图12
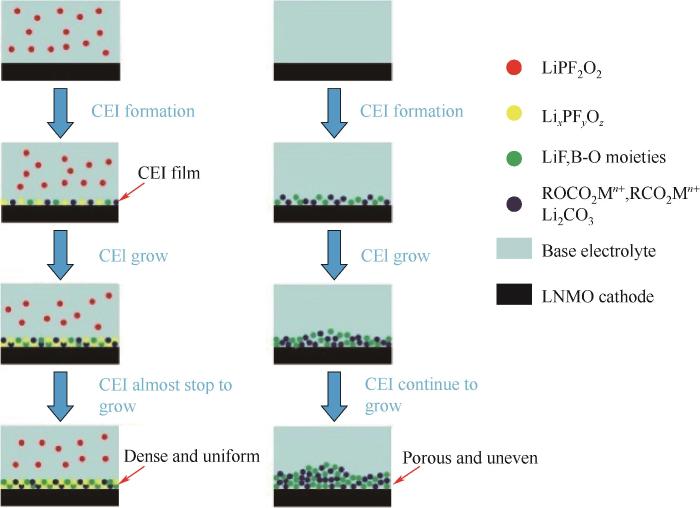
图12 LiPO2F2参与CEI膜形成的机制[119]
Fig.12 Mechanism of the LiPO2F2 participating in the formation of CEI film[119]
LiPO2F2除了具有优异的成膜能力之外,其具有的高压稳定性和高低温性能也值得被关注[120-121]。除了上述锂盐类成膜添加剂外,文献报道较多的还有LiTFOP、LiTFSI、LiFSI、LiBODFP等新型锂盐。Qin等[122]研究了LiTFOP作为电解质添加剂的性能,添加LiTFOP后,电池的容量保持率和安全性显著提高,而且降低了循环过程中的阻抗增长速率。Song等[123]使用LiBODFP作为电解质添加剂,研究发现这种添加剂可以抑制电解液的氧化分解,形成具有更多LiF的SEI薄膜。由于LiF具有较高的杨氏模量,因此SEI薄膜将会变得更加致密。Wang等[124]则采用一种简便、通用的方法合成了二氟LiBODFP和LiTFOP的螯合锂盐,二者的结合能够显著降低界面阻抗。这不仅对新型锂盐的分子设计具有重要的参考意义,而且对构建与不同电极材料兼容的电解液体系也具有重要意义。Wang等[125]系统地研究了LiODFB、LiBOB、LiBODFP和LiPO2F2作为电解液添加剂对LiMn2O4电极的影响。研究发现LiBOB或LiDFOB中的BOB-阴离子与溶解的Mn2+结合,在电极表面形成不溶且稳定的SEI膜,抑制了LiMn2O4在循环过程中的分解,而LiDFOB不仅提高了循环性能,还提高了高温速率性能。通过对石墨电极的XPS和阻抗谱进行测试,Sharova等[126]发现与使用VC获得的SEI相比,在酰亚胺盐存在下获得的SEI更薄,包含更多的LiF且阻抗更小。
锂盐类成膜添加剂不但能够在循环过程中对电极材料的SEI膜形成进行优化,还能够起到传输Li+的作用。这既提高了电池的循环性能、抑制了电解液的氧化分解,又提高了电池的放电容量和库仑效率。虽然LiPF6有对水敏感和高温性能差等缺点,但是其至今仍在电解液中占有主要地位。为了克服这些问题,一方面,在LiPF6地位不变的情况下,筛选出新型的辅助型锂盐作为添加剂,与LiPF6联合使用抑制其在循环过程中的分解,减少其自身的缺点所带来的问题;另一方面,研发出能够完全取代LiPF6的高性能、低成本的新型锂盐,从而获得价格低廉、热稳定性强、电导率高、与隔膜/电极材料兼容性强的电解液。
2.4 无机化合物类添加剂
自从Aurbach等[127]提出以CO2作为电解液添加剂之后,各种无机化合物添加剂逐步走进了科研人员的视线。无机成膜添加剂主要包括CO2、SO2、Na2CO3、Na2SO3、K2CO3等。CO2被有机电解液饱和时,高电位下能够在石墨电极反应生成Li2CO3,这会很好地钝化石墨负极,改善石墨负极的循环性能、放电倍率和电化学稳定性等。Krause等[128]研究发现与含有FEC电解质的电池相比,含有CO2的电池显示出更低的寄生热功率、更好的库仑效率和更好的容量保持率,CO2被证明是无EC电解液中石墨的有效SEI形成剂。Schwenke等[129]研究表明添加CO2有利于SEI的形成。其形成机理是CO2与水和HF结合,形成由甲酸锂和碳酸锂构成的第一钝化层,该钝化层可以抑制溶剂的后期分解。Yu等[130]利用FTIR来精确测定各种碳酸酯基电解液中的CO2含量,结果表明,CO2在含1 mol/L Li+的EC/DEC[1∶2 (体积比)]溶液中的溶解度显著依赖于盐阴离子,混合非极性溶剂也有利于CO2的溶解,如图13所示。FTIR方法非常适合于快速评估CO2在不同电解质体系中的溶解度,这有助于快速开发锂离子电池高性能电解液。
图13
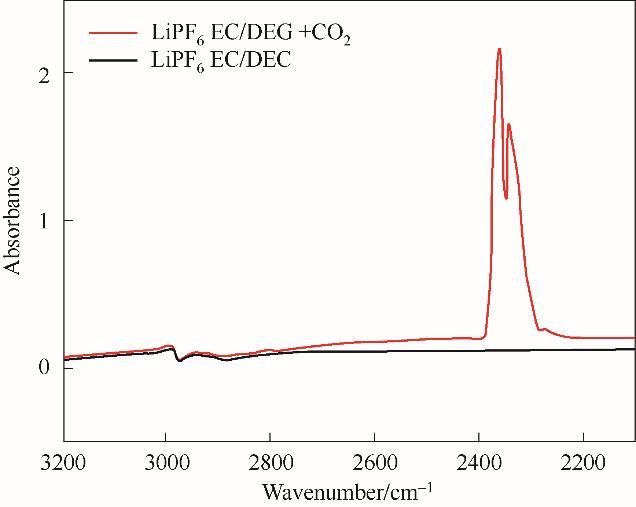
图13 1 mol/L LiPF6在无CO2和CO2饱和的EC/DEC溶液中的红外光谱[130]
Fig.13 IR spectra of 1 mol/L LiPF6 in EC/DEC solutions without CO2 and saturated with CO2[130]
SO2作为成膜添加剂主要是因为SO2为极性分子,因此在有机溶剂中要比CO2的溶解度大,降低了有机溶剂的黏度,提高了离子电导率;其次由于SO2能够起到和CO2类似的有助于形成稳定石墨电极的作用,即使非常低浓度的SO2作为添加剂时,也能够在石墨电极上形成充分发展的钝化膜,且其电位远高于电解液还原本身的电位[131]。这些石墨表面薄膜由SO2和溶剂还原产物的混合物组成。Zhang等[132]研究了电解液中SO2和CO2作为成膜添加剂对石墨电极的影响,发现两种添加剂均能促进石墨阳极表面形成良好的SEI膜,从而获得良好的循环性能,但其内阻、热稳定性、低温性能没有显著变化。虽然气体类添加剂能够明显改善石墨阳极的电化学性能,有助于形成稳定的SEI膜,但其溶解度和其他成膜添加剂相比仍是较小的。另外,气体类添加剂会导致电池内部压力过大,容易造成安全隐患,导致气体类添加剂逐渐淡出了科研人员的视线。
其他的无机化合物类添加剂还有CS2、Na2CO3、K2CO3、NaClO4、Li2CO3、Na2SO3、AgPF6等。李佳等[133]在1 mol/L LiPF6/EC+DMC的电解液中加入Na2CO3,发现添加饱和Na2CO3可促进在石墨电极表面形成更稳定的SEI膜,抑制循环过程中电解液的进一步还原分解,增进Li+嵌脱过程的可逆性。Zhuang等[134]研究发现K2CO3能够成功地将SEI膜改性为具有更好黏弹性的蠕虫网状结构,以适应电化学循环过程中石墨电极的体积变化,并使锂离子更容易插入石墨电极和从石墨电极上脱层,从而有助于提高石墨电极的性能。Wu等[135]将AgPF6-LiNO3添加剂引入碳酸酯电解液中,发现可诱导在锂金属表面形成均匀致密的Ag-Li合金晶种层,如图14所示。这种致密的Ag-Li合金晶种层的出现对Li枝晶的均匀形核和生长起到了积极作用,并且LiNO3可以抑制Li的生长,并在循环过程中起到细化晶粒的作用,从而使锂阳极在循环过程中的结构稳定性和长期循环性能得到显著改善。
图14
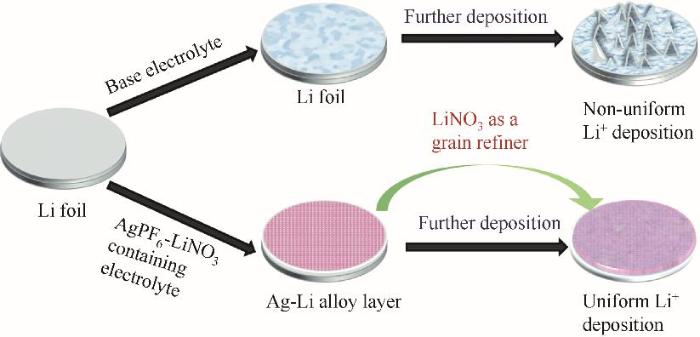
图14 裸锂箔和均匀Ag-Li合金层上Li形核和生长过程的示意图[135]
Fig.14 Schematic diagrams of the Li nucleation and growth process on the bare Li foil and uniform Ag-Li alloy layer[135]
由于无机添加剂本身不可燃,相对于易燃的有机溶剂,提高了锂离子电池的安全性。但是无机添加剂的溶解度比有机添加剂要低得多,因此其应用很少。无机添加剂主要对SEI膜起到修饰作用,对SEI膜的结构进行改性,使得电极表面的形貌变得更加平整光滑。按照成膜机制可以大致分为:能够稳定石墨负极,提高与石墨电极的兼容性的无机类添加剂,如CO2、SO2等;能够抑制锂枝晶的生长,防止溶剂进行共嵌和石墨剥落的添加剂,如AgPF6、LiNO3等;降低电解液中HF的含量,提高循环性能和安全性的添加剂;降低电解液黏度的添加剂等[7,136-138]。无机钠盐和钾盐用作成膜添加剂时的成膜效果是比较显著的,而且该类碱金属盐廉价易得,是值得进行推广的无机添加剂。
2.5 其他添加剂
其他的成膜添加剂还有硅烷类添加剂、GBL及其衍生物、离子液体、酸酐类添加剂以及含氮类添加剂等,文献报道过该类添加剂的成膜效果。大多数的硅烷类添加剂由于含有Si—O键而能够被优先还原,从而抑制了电解液的分解。Lee等[139]观察到TPFPS的优先还原现象,在石墨电极首次锂化后,添加TPFPS的电极形成的SEI层致密且均匀,而且抑制了后续的电解液的分解。Wang等[140]研究了VTMS作为成膜添加剂在Si/C阳极上的效果,VTMS有助于在阳极表面形成稳定的SEI,因此Si/C阳极的容量和可循环性得到改善。Yue等[141]使用三(五氟苯基)硼烷(TPFPB)作为锂金属电池的添加剂,由于TPFPB具有缺电子特性,因此可以作为阴离子受体来吸引
Shen等[143]使用琥珀酸酐(SA)作为碳酸酯电解液中的添加剂显著提高了Li/NCM811电池的循环性能和速率能力。这主要归因于在颗粒上形成均匀的导电阴极CEI层。SA形成的CEI可以保护NCM811表面的活性位点免受副反应的影响,坚固的CEI层可以抑制NCM811的内部裂纹,阻止不可逆相变和镍元素迁移。Wang等[144]使用靛红酸酐(IAn)在NCM523阴极和石墨阳极上构建了稳定的SEI膜。电化学测试表明,IAn可以显著提高石墨/NCM523全电池在高压和高温下的长期循环性能。这种电化学性能的明显改善是由于在两个电极表面形成了薄而稳定的SEI膜,从而抑制了电解质分解,保护了阴极和阳极上的材料结构。Zhang等[145]合成了一种新型离子液体N-丁腈-N-甲基哌啶双(氟磺酰)酰亚胺(PP1,CNFSI)。研究表明,PP1,CNFSI的加入促进了SEI膜的形成,从而抑制了电解质的氧化分解,保护了阴极材料的结构。Lee等[146]使用己二腈作为富镍NCM/Li电池体系的添加剂,发现己二腈可有效稳定锂金属阳极和富镍NCM阴极界面。这项工作为使用高效电解质添加剂开发高性能富锂/富镍NCM电池开辟了一条新的途径,该添加剂可以有效稳定锂金属/电解质和富镍阴极/电解质界面。
3 未来成膜添加剂的研究思路
根据上述的总结和概括,作者认为在未来开发成膜类添加剂的主要思路有:
(1)添加剂应以有机物种为主,能够形成弹性模量小的SEI膜,便于适应阳极材料产生的膨胀行为。
(2)添加剂要尽量保证形成的SEI膜与石墨等阳极材料产生良好的黏结,因此添加剂形成的聚合物的聚合度不能太小。除此以外,添加剂还要有较宽的电化学窗口,避免SEI的持续生成。
(3)在没有性能极其优秀的成膜添加剂出现之前,添加剂的分子结构可以在现有的添加剂的基础上进行结构的优化或者官能团的设计,如FEC或VC之于EC,PES之于PS,DTD之于ES,LiODFB之于LiBF4和LiBOB,LiTFSI之于LiFSI等。这些成膜添加剂都是在传统的溶剂或者添加剂的基础上进行改进优化的,实验证明优化之后的添加剂分子往往要比传统的添加剂具有更好的成膜能力,能够使得锂离子电池的循环寿命和容量得到提高。
(4)尽管使用计算模拟的方法能够快速筛选合适添加剂,但是能够真正规模化应用的添加剂可谓寥寥无几。因此未来应当转变思路,重点攻克当前添加剂的应用问题,提高添加剂的合成技术,降低合成成本,便于大规模的应用,造福社会。
4 结 论
锂离子电池因其具有高电压、高容量、体积小等优势,当前已经在储能领域占有很重要的位置。但随着科技的不断发展,人类生活水平的大幅度提高,对锂离子电池也提出了更高的要求。目前仍在努力开发的高能量密度锂离子电池所产生的各种科学和技术挑战需要进一步解决。电解液和电极之间形成的SEI膜仍需进一步改进,以抑制有害的界面反应,并确保Li+易于迁移[147-150]。锂离子电池添加剂因其使用量小但对电池性能提升显著的特点得到了科研人员的广泛研究。作为锂离子电池中“最重要但是了解最少”的一个部分,良好的SEI或CEI膜对于改进电池技术至关重要。本文综述了近五年来不饱和酯类添加剂、含硫添加剂、锂盐类添加剂、无机化合物类添加剂和其他成膜添加剂的研究进展。
总地来说,成膜添加剂可分为阳极成膜添加剂和阴极成膜添加剂。对于阳极侧,添加剂的还原电位需要高于电解液,便于在循环过程中优先于电解液发生还原,形成稳定的SEI膜。对于石墨阳极,形成稳定的SEI膜的主要阻碍是溶剂的共嵌入和Li+在低电位嵌入/脱出石墨电极的热力学不稳定性;对于Si/C复合阳极或Si电极则是会产生大体积膨胀和内部硅材料破碎;对于锂金属阳极则是会形成树枝状枝晶,过长的枝晶可能会刺穿隔膜造成短路而产生危险。对于阴极侧,添加剂的氧化电位要低于电解液,使得在循环过程中能够优先于电解液发生氧化,形成电导率高的CEI膜。对于阴极侧形成稳定SEI膜的主要障碍是阴极材料中过渡金属的溶解和阴极材料的氧化分解、机械断裂等。
综上,根据文献总结出选用成膜类添加剂所需要注意的方面:第一,筛选阳极添加剂时添加剂的还原电位要高于电解液,而在选用阴极添加剂时添加剂的氧化电位要低于电解液,目的是让添加剂先于电解液发生氧化还原反应,从而优先参与到SEI膜的形成过程中。第二,由于在形成SEI膜的过程中不可避免的Li+损失,导致电池的充放电效率和循环性能下降,因此添加剂应能够防止SEI膜的持续生成。第三,SEI膜的外层主要是有机溶剂的氧化分解产物,结构疏松多孔,是形成形貌均匀、光滑平整的SEI膜的主要障碍。因此添加剂应有聚合能力,便于形成形貌平整、成分均匀的SEI膜,使得SEI膜具有良好的热稳定性和循环性能。第四,由于添加剂的用量对SEI膜或CEI膜的形成有重要影响,如VC,因此在筛选添加剂时,应同时考虑其氧化性质和还原性质。第五,添加剂反应之后得到的副反应产物不能和Li+发生反应,防止Li+的二次损失,能够在提高Li+电导率的同时降低SEI膜的阻抗。除此之外,最好能够吸收循环过程中生成的有害HF。第六,应考虑添加剂与电池其他组分之间的兼容性,如电极材料、电解液甚至是隔膜之间的反应性。第七,可以在已有的添加剂的基础上引入合适的官能团来得到需要的性能,如与EC 结构类似的VC, 其中的碳碳单键改变为碳碳双键之后, 成膜性能变好;而用F 取代 EC得到的FEC, 不但氧化稳定性增强,而且增强了与石墨阳极的兼容性。因此具备多种官能团的添加剂能够满足电解液的多功能需求,对电解液进行多方面的改善。
通过科研人员的不断努力,最近几年已经报道了许多新型的成膜添加剂,尽管添加剂的成分不尽相同,但总的研发思路却是大同小异,即在传统添加剂基础上,不断尝试调整电解液的各项成分的比例,并使不同种类的添加剂进行优势互补。本文提出了今后开发成膜类添加剂所要重点关注的几个方面。
(1)由于单一的添加剂不能同时兼顾电解液的多功能指标,因此未来使用多元添加剂或设计具有多个官能团的新型添加剂是大势所趋,用以弥补单一添加剂在某些方面的短板,便于实现功能上的优势互补。理想的改进可以将几种添加剂组合在一起,前提是它们不会相互干扰。
(2)量子化学计算方法是筛选成膜添加剂的高效方法,可以通过DFT等理论方法进行建模分析、分子设计来筛选合格的成膜添加剂,还可以获取反应产物以及它们如何影响界面性质的信息,这有助于科研人员深刻了解电解液与电极界面之间的作用机理。因此理论与实验相结合的方法无疑是未来筛选添加剂的高效手段。
(3)对SEI膜的表征手段需要进一步提高,考虑到SEI界面对空气的敏感性,在没有干扰的情况下研究界面的形成是非常困难的。为了进一步研究添加剂的作用机理,迫切需要使用原位操作技术。因此在未来的表征过程中可以考虑原位分析方法,如光谱技术、质谱技术和微区电化学技术等。
- 我用了一个很复杂的图,帮你们解释下“23版最新北大核心目录有效期问题”。
- 重磅!CSSCI来源期刊(2023-2024版)最新期刊目录看点分析!全网首发!
- CSSCI官方早就公布了最新南核目录,有心的人已经拿到并且投入使用!附南核目录新增期刊!
- 北大核心期刊目录换届,我们应该熟知的10个知识点。
- 注意,最新期刊论文格式标准已发布,论文写作规则发生重大变化!文字版GB/T 7713.2—2022 学术论文编写规则
- 盘点那些评职称超管用的资源,1,3和5已经“绝种”了
- 职称话题| 为什么党校更认可省市级党报?是否有什么说据?还有哪些机构认可党报?
- 《农业经济》论文投稿解析,难度指数四颗星,附好发选题!
- 期刊知识:学位论文完成后是否可以拆分成期刊论文发表?
- 号外!出书的人注意啦:近期专著书号有空缺!!

 0373-5939925
0373-5939925 2851259250@qq.com
2851259250@qq.com



