甲醇体系电镀污泥衍生磁性多金属材料催化糠醛加氢转化
随着化石能源日益枯竭以及使用过程引起的环境污染和气候恶化,造成经济和社会的可持续发展面临严峻挑战,在资源和环境的双重压力下推动了人们对清洁可再生资源的开发和利用。利用农林废弃物类生物质转化的生物基化合物来高效、经济地制备高品位燃料或高附加值精细化学品,逐渐成为当今科学界和工业界研究的热点[1-3]。在众多生物基平台化合物中,生物质酸催化降解或低温热解产物糠醛(FFR)因其独特的结构特点[4],可通过加氢/氢解转化合成一系列高附加值呋喃衍生化学品,如糠醇(FA)、四氢糠醇、2-甲基呋喃(MF)、戊二醇等。其中,FA可用于生产呋喃树脂、合成纤维、橡胶等,而MF既可作为医药行业有机合成中间体,又能够作为添加剂以提高汽油辛烷值[5-7]。
生物基FFR主要通过催化加氢或加氢脱氧方式转化获得FA和MF。目前常用的催化剂包括廉价的铜、镍基过渡金属,以及钌、铂、钯等贵金属,如Ni-Cu/SiO2[8]、Cu/SiO2[9]、Ru/SiO2[10]、Pd/TiO2[11]、Pt-Co/TiO2[12]、Pt3Fe/CeO2[13]等。Panpranot等[12]采用火焰喷涂法合成负载型铂钴双金属催化剂用于FFR低温加氢,其中Co负载量(质量分数) 0.2%的Pt-0.2Co/TiO2在甲醇溶剂中表现出较优的催化加氢活性,在2 MPa H2环境经过50℃反应2 h,FFR几乎完全转化,FA选择性达97.5%。Weerachawanasak等[8]以SiO2负载镍铜双金属催化FFR加氢,结果表明,双金属催化剂比单金属的2%Ni/SiO2和2%Cu/SiO2具有更优催化加氢活性;在20 bar (1 bar=105 Pa) H2、100℃条件反应2 h,2%Ni-5%Cu/SiO2催化FFR加氢转化率达94%,FFA选择性为64%。Gao等[13]以CeO2负载铂铁合金粒子用于氢气气氛FFR转化,在Pt3Fe/CeO2催化作用下,FFR加氢初始反应速率和FA选择性分别达到1495 h-1和100%。上述研究均以纯氢作为氢源用于FFR转化,但是氢气成本较高、储存运输安全性要求高,故而研究人员探索开发各类有机氢供体用于FFR加氢,包括低碳醇(甲醇、乙醇、异丙醇、正丁醇)、硅烷、甲酸及其盐类等[14-16]。其中,甲醇重整制氢副产物主要以气态CO2形式存在,并伴有少量CO、CH4产生,故不会残留在反应液中,且对后续FFR加氢转化过程无影响[17]。目前,利用甲醇重整制氢用于FFR原位加氢转化已有研究报道。Zhang等[18]将Pt纳米粒子负载于类钙钛矿MgTiO3,制备的Pt@MT-450在120℃催化FFR转化得到75.5%FA。Zhang等[19]以水滑石为前体合成一系列铜基催化剂用于甲醇体系FFR转化,结果表明,在200℃反应2.5 h后FA收率为94%,进一步提高反应温度至240℃,则逐步向脱氧产物MF转化,其最高收率达到94.1%。上述报道使用的催化剂均以过渡金属为活性中心,可实现FFR的选择性加氢转化。
近年来,研究人员发现以电镀行业产生的含有多种过渡金属的污泥作为前体,经过煅烧及后续改性处理,获得的多金属材料亦可应用于各类催化反应中。例如,Shen等[20]采用电镀污泥为前体合成含铬尖晶石以进行选择性催化还原去除NO,其中CuCr2O4和NiCr2O4两类含铬尖晶石在225℃对NO去除率分别为88%和60%。Bai等[21]采用La和Ca对煅烧后含铬电镀污泥进行改性,合成的钙钛矿型催化剂La1-x Ca x CrO3在VOC催化氧化过程表现出良好的反应活性,其在302℃催化甲苯脱除率达到50%。由此可见,电镀污泥中的金属组分可作为催化反应重要的活性中心。
鉴于此,本文拟以含铜、铁等过渡金属的电镀污泥为前体,经煅烧处理合成磁性多金属催化材料,探讨其在甲醇供氢体系催化生物质基FFR加氢转化性能,系统研究电镀污泥煅烧温度、反应工艺条件等影响,并结合表征结果对电镀污泥衍生磁性材料催化反应性能进行分析讨论。
1 实验部分
1.1 实验化学药品
实验所用FFR(AR,99%)、FA(AR,98%)和MF(AR,98%)均购自上海晶纯试剂有限公司。甲醇(AR,99.5%)来源于广州化学试剂有限公司。
1.2 催化剂制备
实验所用电镀污泥取自广州某电镀厂,收集的污泥样品首先在105℃下过夜干燥,粉碎筛出粒径小于160 μm的颗粒。然后将过筛样品置于管式炉(KSY-6-16 A,天津中环电炉有限公司)中,以10℃/min升温速率,分别在空气气氛400、550、700和850℃下煅烧4 h,煅烧后的电镀污泥样品简记为CES-T,T代表电镀污泥煅烧温度。其中,对于重复使用后的CES-700催化剂简记为CES-700R。
1.3 催化剂表征
电镀污泥金属元素组成及含量由帕纳科公司AXIOS mAX petro X射线荧光光谱仪测定。煅烧后电镀污泥物相结构表征采用帕纳科公司X’Pert Pro MPD型X射线衍射仪进行测定,辐射源Cu Kα,管电压40 kV,管电流40 mA,扫描速度0.1 s/步。采用美国Quantachrome公司全自动多站物理吸附仪(介孔)QUDRASORB SI-MP-10测定煅烧后电镀污泥的比表面积和孔隙结构。测试前样品在210℃下真空脱气8 h,以Brunauer-Emmett-Teller (BET)方法计算样品比表面积,应用Barret-Joyner-Halenda (BJH)方法获得样品孔径信息。
采用美国Micromeritics公司AutochemⅡ 2920 Chemisorption测定煅烧后电镀污泥表面酸性。称取约100 mg样品置于U形管中,以10℃/min从室温程序升温至300℃进行预处理,以30 ml/min 氦气吹扫1 h,冷却至50℃,通入8% NH3-He混合气(50 ml/min) 1 h至饱和,切换He气流吹扫1 h除去表面物理吸附的NH3,最后在氦气气氛以10℃/min升温至1000℃脱附,保持30 min,用TCD检测脱附的NH3。采用日本Hitachi公司扫描电镜S-4800观察煅烧后电镀污泥颗粒形貌。在美国Thermo Fisher Scientific公司ESCALAB 250Xi型X射线光电子能谱仪上测定煅烧后电镀污泥的XPS谱,光源为Al Kα,以C 1s的结合能 (284.6 eV)为基准校准Cu、Fe元素的电子结合能。采用德国NETZSCH公司STA 449 F5+QMS同步热分析-质谱联用仪测定使用后催化剂的积炭情况。以10℃/min的升温速率,在50 ml/min空气环境升温至700℃,同时质谱m/z值设定为18、32和44。
1.4 催化剂性能测试
将煅烧后电镀污泥、甲醇(12 ml)和FFR (0.6 mmol)置于100 ml高压反应釜中,密封高压反应釜,用N2置换3次后充入保护性N2至1 MPa,升温至设定反应温度。反应结束后,将高压反应釜降至室温,液体产物经0.45 μm微孔滤膜过滤后进行定性定量分析。
采用气相色谱-质谱联用仪(Thermo Scientific Trace 1300-ISQ 7000,GC-MS)对反应后液体进行检测。检测色谱柱为Agilent DB-1701毛细管柱(50 m
2 实验结果与讨论
2.1 催化剂表征
表1所示为电镀污泥中元素组成,其中金属元素Fe、Cu占主要部分,质量分数分别高达44.57%和30.28%,故煅烧后电镀污泥具有较强磁性,利于反应后回收再用,同时又含有催化甲醇重整制氢和FFR加氢转化所需的Cu组分。
表1 电镀污泥主要元素成分
Table 1
| 组成 | 质量分数/% |
|---|---|
| Fe | 44.57 |
| Cu | 30.28 |
| O | 14.28 |
| Ni | 2.51 |
| Sn | 2.35 |
| S | 2.04 |
| Si | 1.04 |
| Ca | 0.96 |
| 其他 | 1.97 |
新窗口打开| 下载CSV
对煅烧后的电镀污泥样品CES-T进行X射线衍射(XRD)表征,结果如图1所示。当煅烧温度为400℃时,样品中的金属组分多以非晶相存在,仅观察到微弱的Fe2O3和CuO衍射峰[22]。提高煅烧温度至550℃以上,电镀污泥中的金属组分逐步向晶相转化,出现一系列金属氧化物和尖晶石类化合物特征峰。其中,衍射峰2θ值在18.2°、30.1°、35.3°、37.0°、43.2°、57.2°、62.8°和75.0°,分别对应立方晶系CuFe2O4的(111)、(220)、(300)、(222)、(400)、(511)、(440)和(533)晶面;位于21.1°、33.1°、35.5°、49.4°、62.8°和63.9°处的衍射峰对应三角晶系Fe2O3的(012)、(104)、(110)、(024)、(116)、(214)晶面,38.7°、48.7°、66°处的衍射峰则可归为CuO(111)、(-202)和(-311)晶面。在26.6°、33.9°和51.8°处的衍射峰则对应SnO2(110)、(101)和(210)晶面。因镍氧化物和尖晶石特征衍射峰与CuFe2O4的2θ值接近,故煅烧后样品中Ni组分可能以NiO和NiFe2O4形式存在[23]。对重复利用催化剂CES-700R的XRD谱图进行分析发现,Fe2O3对应的(012)、(104)、(024)、(116)晶面在循环使用过程逐步消失,这可能是由于在高温甲醇重整产氢环境易引起部分高价态Fe3+转变为低价态Fe2+。
图1
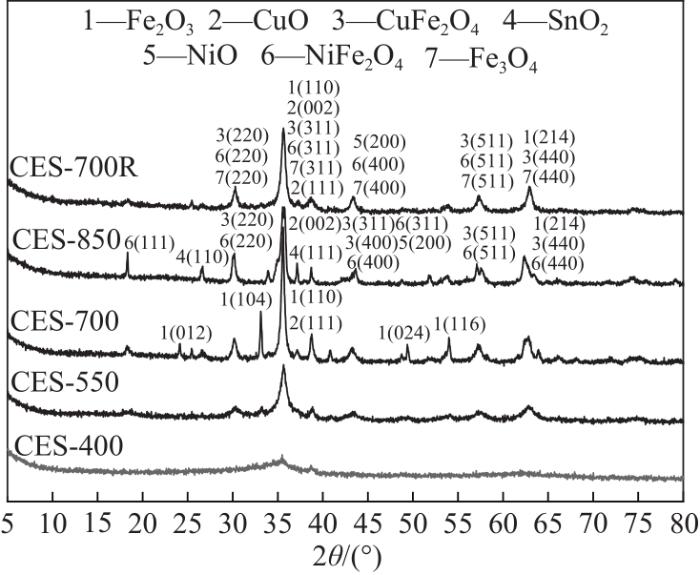
图1 煅烧后电镀污泥XRD谱图
Fig.1 XRD patterns of calcined electroplating sludge
CES-T样品液氮吸脱附表征曲线如图2所示,四种不同煅烧温度制备的催化剂均表现出H4滞后环和Ⅳ型等温线,表明CES-T样品均具有部分介孔结构。表2对样品比表面积、孔径和总孔容进行总结,结果表明,随着煅烧温度由400℃提高至850℃,比表面积、平均孔径和总孔容逐渐降低,其中比表面积由82.53 m2/g降至10.14 m2/g,总孔容由0.34 cm3/g 降至0.02 cm3/g,表明煅烧处理让污泥中的絮状沉淀金属氢氧化物变成氧化态,产生介孔结构,继续提高煅烧温度则导致孔道坍塌、介孔部分消失。对于循环使用的CES-700R催化剂,其比表面积由41.10 m2/g降至25.47 m2/g,孔径由54.05 nm降为3.86 nm,这主要是由于反应过程CES-700催化剂出现颗粒团聚、部分积炭。CES-T样品SEM图(图3)可进一步证明液氮吸脱附表征结果,400℃煅烧的CES样品孔道结构较丰富,类球形和棒状金属氧化物颗粒互相堆积。当CES样品煅烧温度高于550℃时,则样品颗粒开始出现烧结现象,介孔结构被破坏。与新鲜的CES-700催化剂相比较,CES-700R催化剂颗粒呈现无序堆积、团聚现象,且颗粒大小差异较大,而且由于在反应过程中部分Cu金属组分被还原,出现细小的纳米颗粒。
图2
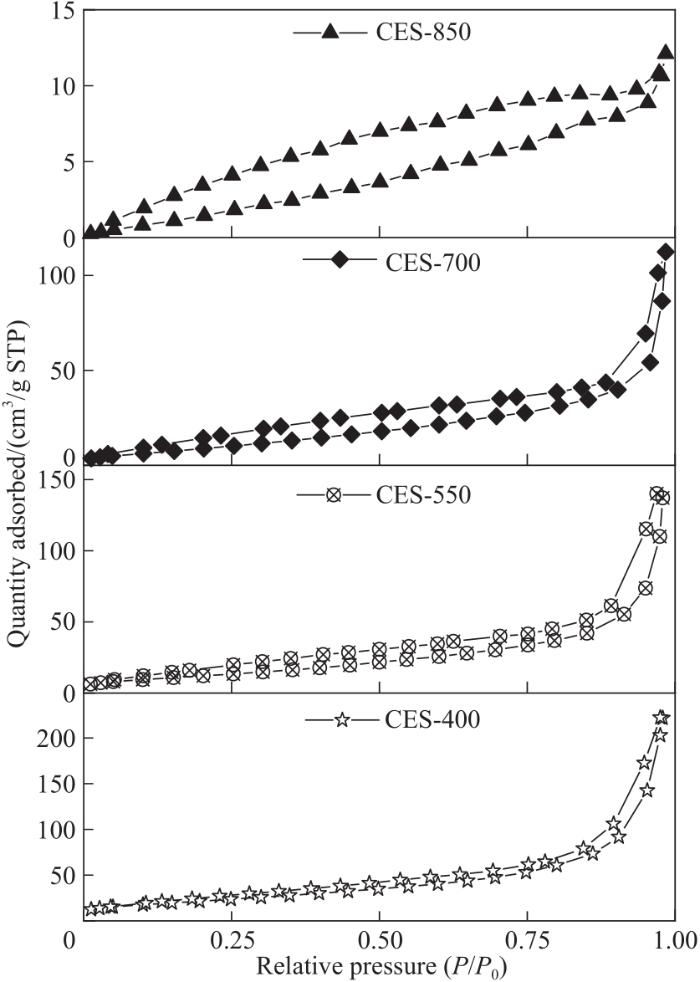
图2 CES-T样品N2吸附-脱附等温线
Fig.2 N2 adsorption-desorption isotherms of as-prepared CES-T
表2 CES-T催化剂结构特性
Table 2
| 样品 | 比表面积/(m2/g) | 平均孔径/nm | 总孔容/(cm3/g) |
|---|---|---|---|
| CES-400 | 82.53 | 29.41 | 0.34 |
| CES-550 | 48.13 | 30.20 | 0.21 |
| CES-700 | 41.10 | 54.05 | 0.17 |
| CES-850 | 10.14 | 3.41 | 0.02 |
| CES-700R | 25.47 | 3.86 | 0.10 |
新窗口打开| 下载CSV
图3

图3 CES-T和CES-700R样品SEM图
Fig.3 SEM images of as-prepared CES-T and CES-700R
NH3分子在催化剂上的解吸温度反映了对应酸性位点的强度,脱附温度越高,说明催化剂酸性位点越强[24]。CES-T样品NH3化学吸附曲线如图4所示,350℃左右出现脱附峰表明部分弱酸性位点存在于CES-T样品中,而在600℃以上出现的脱附峰则表明催化剂存在强酸性位点。四种CES-T样品酸量分布如表3所示,CES-400和CES-550表现出相对较弱的酸量,分别为12.3和10.3 μmol/g。提高煅烧温度有助于强酸性位点的生成,其中CES-700和CES-850强酸量分别高达24.6和18.5 μmol/g。在煅烧温度850℃时,CES-T样品强酸性位点减弱,这主要是由于部分尖晶石结构的形成。
图4
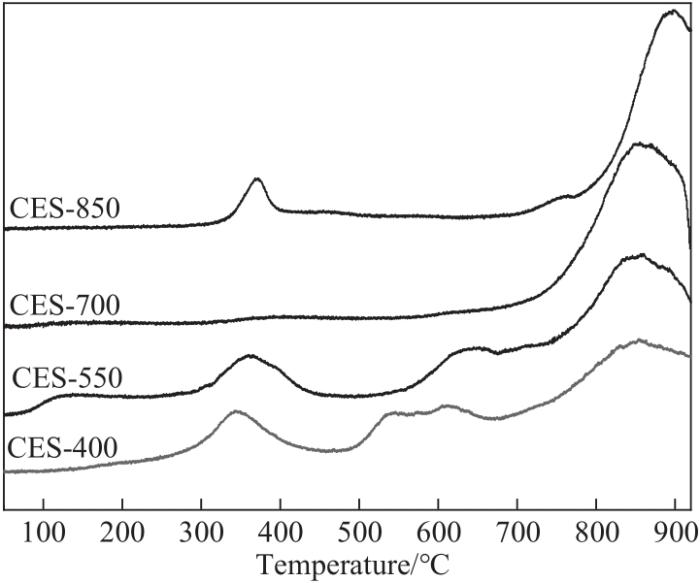
图4 CES-T催化剂NH3-TPD谱图
Fig.4 NH3-TPD profiles of as-prepared CES-T samples
表3 CES-T样品酸性位点分布
Table 3
| 样品 | 弱酸性/(μmol/g) | 中等酸性/(μmol/g) | 强酸性/(μmol/g) | 总酸量/(μmol/g) |
|---|---|---|---|---|
| CES-400 | 1.8 | 2.4 | 8.1 | 12.3 |
| CES-550 | 1.3 | 2.2 | 6.8 | 10.3 |
| CES-700 | — | — | 24.6 | 24.6 |
| CES-850 | 1.9 | — | 18.5 | 20.4 |
新窗口打开| 下载CSV
为了解铜价态对甲醇供氢体系FFR加氢转化的催化作用,采用XPS对新鲜和反应回收后的CES-700进行价态表征。如图5(a)所示,CES-700的全谱包括C 1s、Ca 2p、Sn 3d、O 1s、Fe 2p和Cu 2p。结合能位于933和953 eV处的峰分别对应于Cu 2p3/2和Cu 2p1/2[图5(b)、(c)][25-26],表明新鲜CES-700中的铜元素以二价的形式存在,可归于CuO和CuFe2O4,结果与XRD分析结果吻合。其中,944.3 eV处的峰是Cu2+的卫星峰。反应后回收的CES-700出现Cu0(23.2%),这主要是因为催化剂表面Cu2+被甲醇重整产生的氢气部分还原。其中,如图5(d)、(e)所示,位于855.2和872.4 eV处的特征峰分别对应于Ni 2p3/2和Ni 2p1/2[27],表明新鲜CES-700中镍元素主要以二价形式存在,可能是NiO和NiFe2O4物种,该结果与XRD分析结果吻合。反应后回收的CES-700R中出现少量Ni0(11.5%),这是由于在甲醇重整产氢体系催化剂表面Ni2+部分还原。对于铁元素XPS谱图进行分析[图5(f)、(g)],新鲜CES-700中Fe元素在结合能714.6 eV处的Fe 2p3/2特征峰可分峰拟合为712.0、714.6和717.6 eV三个峰[28-29],其中712.0 eV处特征峰为Fe2+(13.9%),714.6 eV处特征峰为Fe3+(44.1%),717.6 eV处特征峰则是由于Fe3+(34.7%)与羟基自由基结合产生,而在720.1 eV的特征峰可对应于Fe2+(7.3%)的卫星峰。对于反应后的CES-700R催化剂,催化剂表面Fe3+物种占比从44.1%和34.7%分别下降至24.1%和28.2%,而表面Fe2+占比从13.9%和7.3%分别上升至36.2%和11.5%,这表明在甲醇重整产氢体系新鲜CES-700催化剂中的部分Fe3+物种被还原为Fe2+。
图5
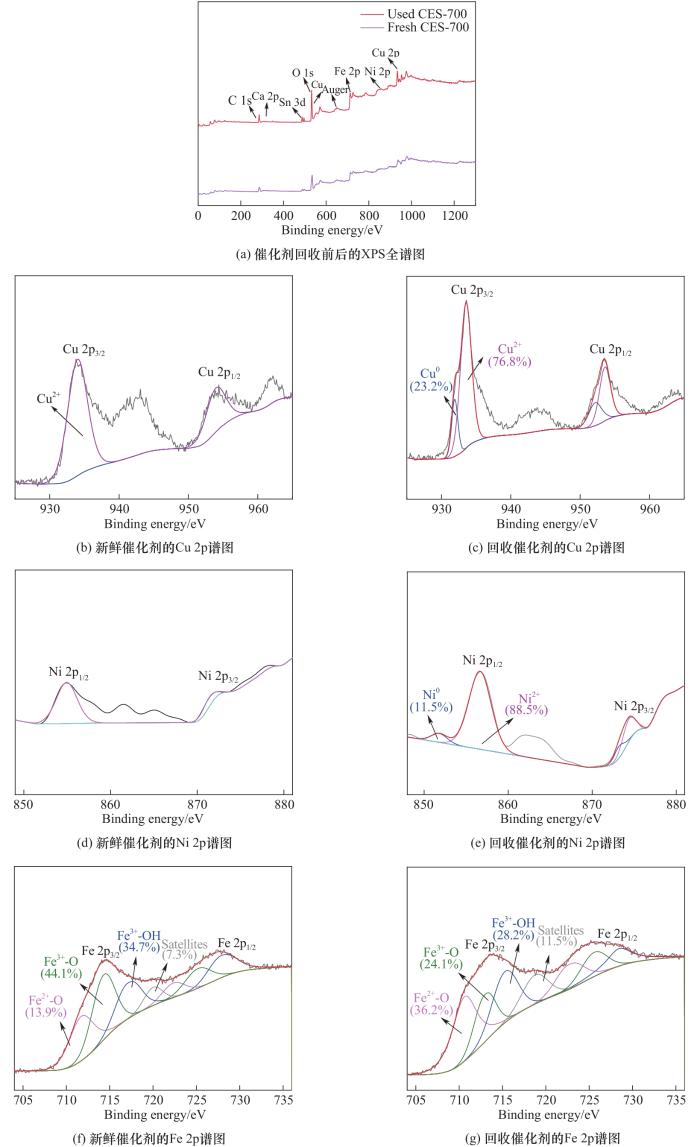
图5 催化剂回收前后的XPS谱图
Fig.5 XPS spectra of fresh and used CES-700
2.2 催化剂性能研究
以CES-700为催化剂,研究其催化甲醇重整产物分布情况,气相产物信息如图6和表4所示。结果表明,甲醇催化重整气体产物主要是氢气,并伴有少量一氧化碳和二氧化碳产生。随后以甲醇为溶剂和氢源,CES-T催化剂在FFR转移加氢中的催化活性结果如表5所示。在400℃煅烧处理的电镀污泥催化作用下,FFR转化率为58.4%,但是FA和MF收率却仅有3.7%和0.8%,这可能归因于催化剂的弱酸位点诱导的平行反应的存在[30],生成部分醚类化合物。另外,低温煅烧的催化剂因具有较低酸性,其在催化甲醇重整供氢方面性能较弱,不能提供足够氢气用于FFR转化反应。当继续提高催化剂煅烧温度至700℃,CES-700催化性能显著增强,FFR转化率高达96.8%,FA和MF收率分别为40.4%和5.9%,这可能是由于CES-700催化剂孔道结构中强酸位点和活性铜物种可以促进甲醇重整供氢,以利于后续FFR加氢转化。当催化剂煅烧温度升至850℃,由于催化剂孔道结构坍塌,强酸位点酸量降低,导致FFR转化率、FA和MF收率均降低。上述结果表明,适当调控电镀污泥煅烧温度可以改善多金属催化剂孔道结构与酸量分布,从而有助于催化甲醇重整产氢和后续FFR选择性加氢转化。综合比较,选择CES-700作为后续甲醇供氢体系FFR加氢转化实验催化剂。
图6
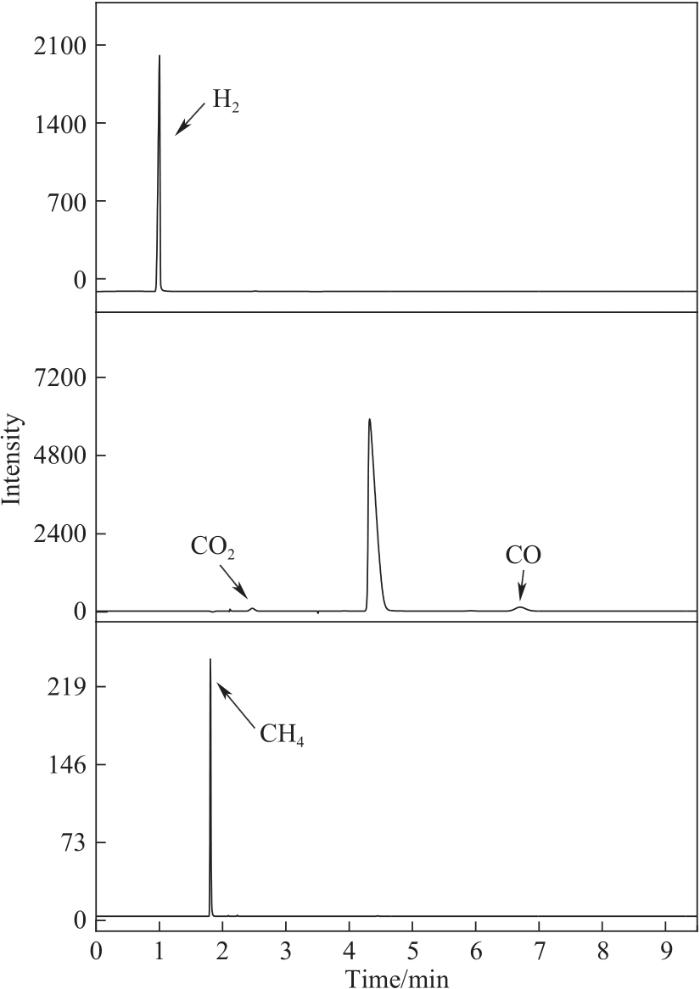
图6 CES-700催化甲醇重整气相色谱图(反应条件:甲醇12 ml,CES-700 30 mg,220℃, 2 h)
Fig.6 GC graph for methanol reforming over CES-700 (reaction conditions: methanol 12 ml, CES-700 30 mg, 220℃, 2 h)
表4 CES-700催化甲醇重整气相产物分布
Table 4
| 保留时间/min | 组分 | 含量/%(体积分数) |
|---|---|---|
| 1.001 | H2 | 11.41 |
| 1.807 | CH4 | 0.20 |
| 2.092 | C2H6 | 0.0003 |
| 2.323 | C2H4 | 0.0005 |
| 2.469 | CO2 | 0.74 |
| 6.702 | CO | 2.57 |
新窗口打开| 下载CSV
表5 CES-T对FFR转移加氢反应的催化活性
Table 5
| 样品 | FFR转化率/% | FA收率/% | MF收率/% |
|---|---|---|---|
| CES-400 | 58.4 | 3.7 | 0.8 |
| CES-550 | 60.9 | 4.1 | 2.9 |
| CES-700 | 96.8 | 40.4 | 5.9 |
| CES-850 | 75.0 | 35.5 | 0.5 |
新窗口打开| 下载CSV
图7所示为反应温度对甲醇供氢体系FFR加氢转化影响。当反应温度为200℃时,FFR转化率为69.5%,FA收率仅为11.6%,几乎没有MF生成,主要副产物为2-(二甲氧基甲基)呋喃(DMF)和2-呋喃甲基甲醚(MFE),如图8所示。这主要是由于低温不利于甲醇重整产氢,无法提供足够氢气用于FFR加氢转化,因而造成加氢产物FA和MF收率较低。升高温度至210℃,FFR转化率达到94.9%,FA收率38.8%,有微量MF产生(约5.9%)。随着反应温度继续升高,FFR转化率均高于95%,同时FA收率开始逐渐减小。这主要归因于高温下甲醇快速分解持续提供氢气,促进催化剂活性位点Cu0的形成,并促进FA加氢脱氧产生MF[31]。温度达到240℃时,FA收率降为31.0%,MF收率达到21.0%。由此可见,FFR在210℃基本就转化完全,继续升高温度可促进FA进一步加氢脱氧转化为MF。综合考虑FFR转化率和加氢产物收率,将240℃作为后续实验的最佳反应温度。
图7
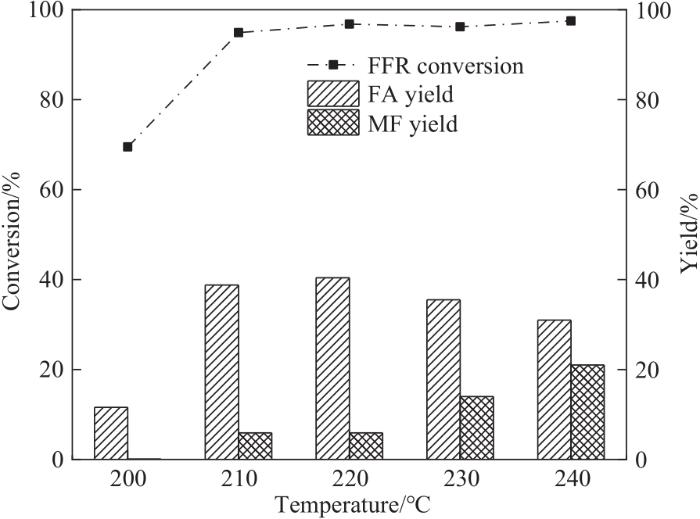
图7 反应温度对FFR加氢转化的影响(反应条件:FFR 0.6 mmol,甲醇12 ml,CES-700 30 mg,2 h)
Fig.7 Effect of reaction temperature on FFR hydrogenation (reaction conditions: FFR 0.6 ml, methanol 12 ml, CES-700 30 mg, 2 h)
图8
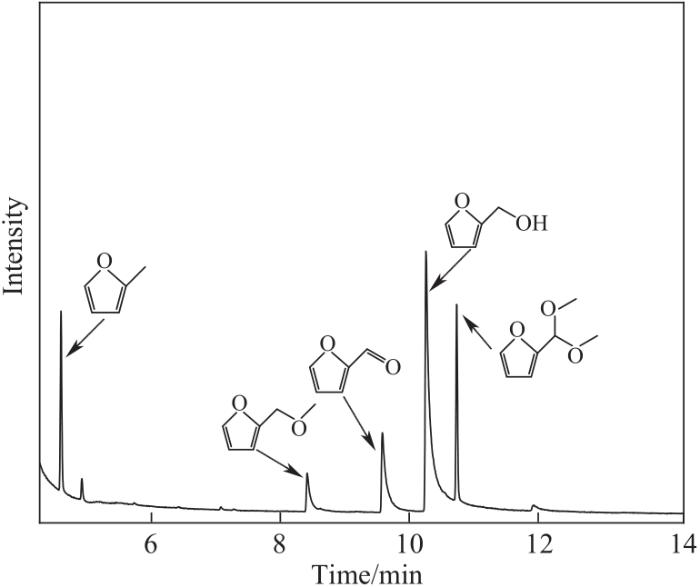
图8 FFR加氢转化产物离子色谱图
Fig.8 The ion chromatogram of obtained products from FFR hydrogenation
图9和图10分别重点考察了CES-700用量和反应时间对甲醇供氢体系FFR加氢转化影响。由图9可知,当催化剂用量为10 mg时,FFR转化率达到89.4%,FA收率为44.1%。增加CES-700用量至20 mg,可显著促进甲醇供氢体系FFR加氢转化,FA收率提高至70.9%。这是因为在相对较短的时间内能产生丰富的活性位点Cu0,有助于甲醇重整产氢和底物FFR加氢转化。随着CES-700用量继续增加,FFR转化率略微上升,且加氢产物FA逐步向脱氧化合物MF转化。在这一转化过程中,催化剂酸性位点可促进部分FA与甲醇发生醚化反应而生成MEF,导致FA收率进一步降低。鉴于FA收率,选择20 mg作为后续实验催化剂用量。图10表示FFR加氢转化随反应时间变化趋势,延长时间有利于FA进一步加氢脱氧生成MF。当延长反应时间至4 h,FFR基本完全转化,其中MF最高收率达到31.9%。因此,适当增加催化剂用量和延长反应时间可提供较多活性金属中心Cu0,并利于FFR和FA与活性位点接触,进而促进甲醇供氢体系FFR加氢转化。
图9
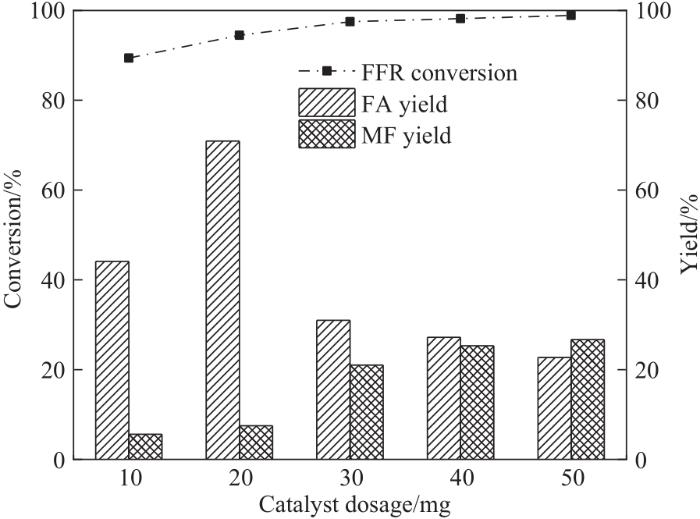
图9 催化剂用量对FFR转移加氢的影响(反应条件:FFR 0.6 mmol,甲醇12 ml,240℃,2 h)
Fig.9 Effect of catalyst dosage on the transfer hydrogenation of FFR (reaction conditions: FFR 0.6 mmol, methanol 12 ml, 240℃, 2 h)
图10
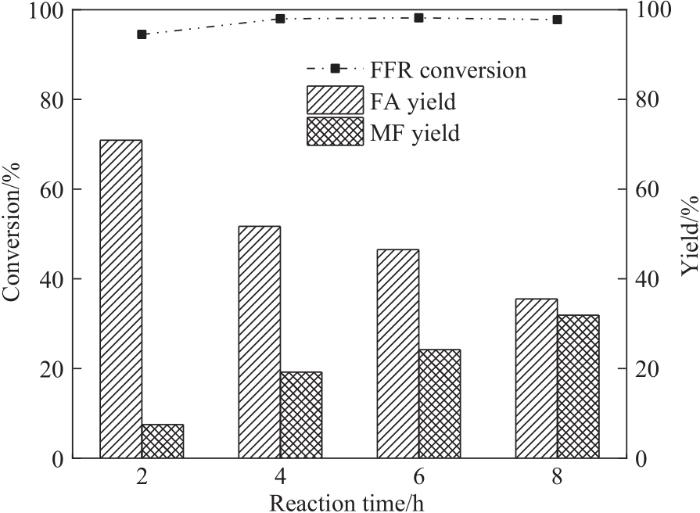
图10 反应时间对FFR转移加氢的影响(反应条件:FFR 0.6 mmol,甲醇12 ml,CES-700 20 mg,240℃)
Fig.10 Effect of reaction time on the transfer hydrogenation of FFR (reaction conditions: FFR 0.6 mmol, methanol 12 ml, CES-700 20 mg, 240℃)
为了探究CES-T催化剂的稳定性和重复使用性能,以CES-700为催化剂,在240℃、用量30 mg、2 h条件下进行循环使用实验。每次反应后,利用磁性回收催化剂,所得样品用无水乙醇洗涤、60℃真空干燥,后经400℃煅烧处理后再次使用。催化反应活性结果如图11所示,循环使用一次后,FFR转化率从97.5%(摩尔分数)降至61.8%,FA收率从31.0%降至26.7%,MF收率由21.0%降至7.8%。继续进行循环实验结果表明其催化活性快速下降,且检测出主要产物为呋喃基醚类化合物。为说明催化剂失活原因,对使用一次后催化剂进行热重表征,其TG曲线如图12(a)所示。从图可知,150℃前催化剂失重为受热脱水阶段,150~350℃质量增加阶段主要为低价态或还原的金属组分被重新氧化。如图12(b)所示,在增重温度区间,O2不断消耗,伴随产生一定量H2O和CO2,表明附着在催化剂表面的有机物开始燃烧,并且在400℃左右位置出现明显CO2释放峰。通过热重结果可以看出,经400℃煅烧处理基本可去除反应后CES-700表面积炭。此外,CES-700在煅烧处理过程易发生颗粒团聚、金属粒子烧结,导致催化剂比表面积、孔容降低,这也是引起其在循环使用过程催化活性显著下降的可能原因。
图11
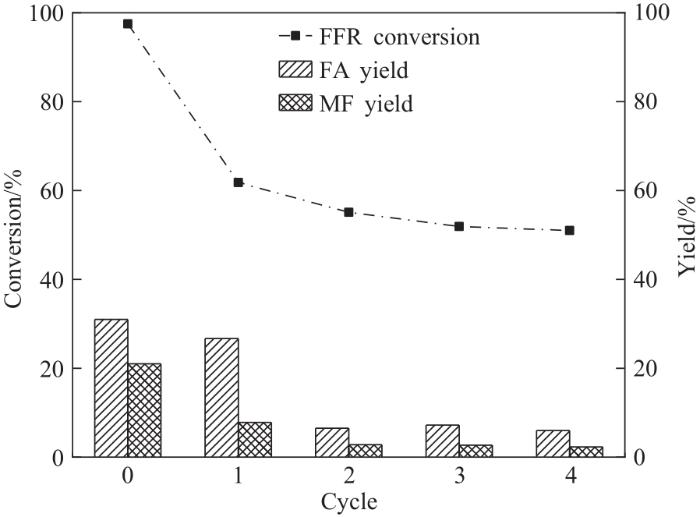
图11 催化剂循环使用性能(反应条件:FFR 0.6 mmol,甲醇12 ml,CES-700 30 mg,240℃,2 h)
Fig.11 Catalyst recycling (reaction conditions: FFR 0.6 mmol, methanol 12 ml, CES-700 30 mg, 240℃, 2 h)
图12
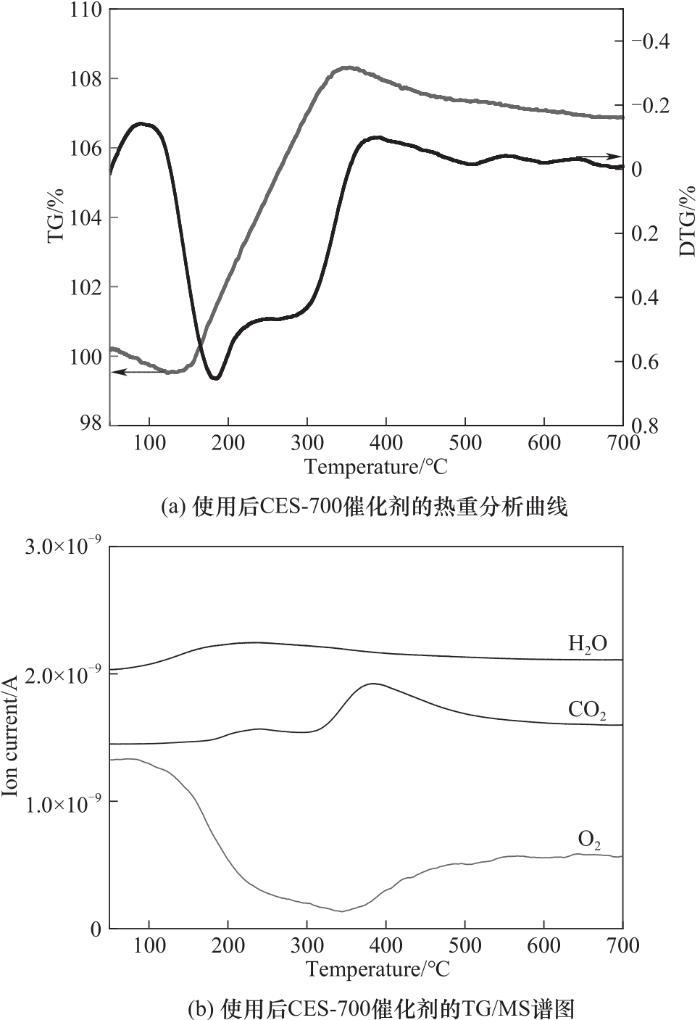
图12 使用后CES-700催化剂的热重特性图
Fig.12 Thermogravimetric characteristics of used CES-700
根据上述实验结果,FFR在甲醇供氢体系加氢转化的可能反应路径如图13所示。因为污泥衍生磁性催化材料含有少量Sn、Ni等金属组分,使得煅烧后的催化剂具有部分Lewis酸(L酸)和Brønsted酸(B酸)性位点,故在上述B酸和L酸性位点作用下,甲醇溶剂首先进行重整反应,生成H2、CO和CO2等。铜氧化物在H2分子作用下被还原为Cu0,而Cu0活性中心又能够促进甲醇重整产氢[32]。随后FFR分子中的C
图13
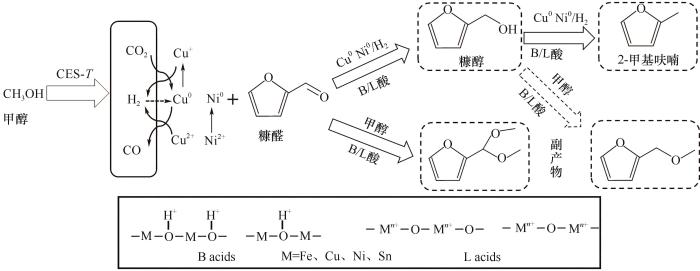
图13 甲醇供氢体系CES-T催化FFR加氢转化反应路径
Fig.13 Reaction path for FFR hydrogenation over CES-T using methanol as hydrogen donor
3 结论
本文以富含铁、铜的电镀污泥为前体煅烧合成磁性多金属催化材料,研究其在甲醇供氢体系生物基FFR加氢转化制备FA和MF的催化性能。研究发现,电镀污泥衍生磁性多金属材料具有强酸性位点和介孔结构,以铜组分为主的活性中心在反应过程中部分被还原为零价,可促进甲醇重整和FFR加氢转化。当以700℃煅烧的电镀污泥为催化剂,在240℃反应2 h以上,FFR转化率接近100%,FA和MF最高收率分别可达70.9%和31.9%,副产物以2-呋喃甲基甲醚和2-(二甲氧基甲基)呋喃为主。同时,基于电镀污泥衍生磁性多金属材料结构中活性金属中心和酸性位点协同作用,甲醇体系FFR转化主要经历甲醇重整产氢、FFR催化加氢至FA以及FA加氢脱氧至MF。
- 刚刚!2026年中科院分区,公布!本次看点:中科院分区变更为新锐分区;不再单独发布预警期刊;37种期刊“under review”~
- 这些重要报纸理论版都支持邮箱投稿!回复极快!
- GB/T 7714-2025与GB/T 7714-2015相比,变更了哪些,对期刊参考文献格式有什么影响?
- 别被这个老掉牙的报纸理论版投稿邮箱误导了!最新核实91个报纸理论版投稿邮箱通道,一次集齐
- 喜报!《中国博物馆》入选CSSCI扩展版来源期刊(最新CSSCI南大核心期刊目录2025-2026版)!新入选!
- 2025年中科院分区表已公布!Scientific Reports降至三区
- 国内核心期刊分级情况概览及说明!本篇适用人群:需要发南核、北核、CSCD、科核、AMI、SCD、RCCSE期刊的学者
- CSSCI官方早就公布了最新南核目录,有心的人已经拿到并且投入使用!附南核目录新增期刊!
- 北大核心期刊目录换届,我们应该熟知的10个知识点。
- 注意,最新期刊论文格式标准已发布,论文写作规则发生重大变化!文字版GB/T 7713.2—2022 学术论文编写规则

 0373-5939925
0373-5939925 2851259250@qq.com
2851259250@qq.com



