木质素羟丙基磺甲基化改性及其对纤维素酶水解的影响
为了减少化石燃料对能源和环境的负面影响,人们对寻求可再生的清洁能源愈发关注[1]。木质纤维原料作为世界上最大的可再生资源,其具有可再生、成本低、易获得等特点,已被广泛用于生物乙醇的生产以替代化石燃料的生产[2]。在木质纤维原料转化为生物乙醇的过程中,酶水解是葡萄糖转化的关键步骤之一,纤维素酶、水解条件、底物等因素都会对酶解效率产生影响[3-4]。底物木质素作为木质纤维原料的主要成分,对酶水解的影响主要表现在木质素引起的非生产性吸附和空间阻碍这两方面,其中纤维素酶与木质素之间的非生产性吸附主要与疏水作用、静电作用、氢键作用有关[5-6]。木质素结构中含有多种官能团,如酚羟基、羧基、甲氧基等,这些官能团使木质素具有疏水性、表面电荷等特性,使之与酶发生相互作用,影响酶水解过程[7-8]。酚羟基被认为是影响木质素抑制作用的关键因素,已有研究表明,木质素模型化合物上的酚羟基会影响纤维素酶的吸附,对其适当的改性可以消除木质素带来的抑制作用[9]。赵存异等[10]对碱木质素进行了羟丙基化改性,研究发现木质素表面特性的改变能够减少木质素对纤维素酶的非生产性吸附。除此之外,常用的改性方法还包括羧化改性,Nakagame等[11]通过研究证实增加木质素的羧酸含量能够显著降低纤维素酶的非生产性结合,从而增加了纤维素的酶水解效率。Yang等[12]也在研究木质素理化性质与抑制纤维素酶解的相关性时发现,分别对木质素进行羧化和磺化改性能够提高木质素的亲水性,将其疏水性降低22%~30%,从而消除木质素76%~96%的抑制作用。木质素的磺化可以减少木质素与纤维素酶之间的疏水作用,降低酶水解过程中底物中木质素对酶的无效吸附[13]。Wu等[14]在实验中发现,在木质素中引入磺酸基团能够提高木质素的亲水性,降低木质素与纤维素酶结合程度的同时能够增强了纤维素的水解能力。也有研究表明,在酶水解体系中加入磺化木质素(sulfonated lignin, SL)后,纤维素酶和SL相互作用形成SL-纤维素酶复合物,从而增强底物木质素与纤维素酶之间的静电斥力,减少纤维素酶对其非生产性吸附[15]。
综上所述,对木质素进行改性获得具有特定性质的木质素是提高纤维素酶与纤维素吸附、增强纤维素酶水解的重要手段。然而现有的改性技术往往只是针对解决疏水作用、静电作用或氢键作用中某一种单一因素,对木质素综合性能提高的改性还亟待进一步的研究。研究木质素的复合改性,将两种或多种改性方式结合起来对减少木质素与纤维素酶之间的非生产性吸附有着重要的作用。本文旨在从疏水作用、静电作用两方面着手从而降低木质素与纤维素酶之间的作用力,通过两步法对木质素进行羟丙基磺甲基化改性,封闭木质素结构中酚羟基的同时引入亲水性的磺酸基团,以期制备一种高负电性、低疏水性的木质素。探究改性木质素对纤维素酶的非生产性吸附及对纤维素酶水解的影响,以期为开发经济、高效的预处理技术提供理论依据。
1 材料与方法
1.1 原料与试剂
木质素原料来源于江苏造纸企业,纯度96.0%。微晶纤维素Avicel PH-101购于Sigma-Aldrich公司。实验所用的纤维素酶(Cellic ® CTec2)购自于丹麦Novozymes公司,滤纸酶活为200 FPU/g,其余化学药品购于国药集团化学试剂有限公司,均为分析纯。
1.2 改性木质素的制备
改性木质素的制备参考文献[9,16]。称取4 g木质素,加入蒸馏水配制成30%(质量)溶液,并用NaOH溶液调节溶液的pH为11。加热至70℃后,加入1 ml 37%的甲醛溶液。反应2 h后升温至95℃,加入1.2 g无水Na2SO3,反应3 h后用0.1 mol/L的HCl调节pH至2,将所得木质素反应产物过滤、水洗、冷冻干燥。取其中固体3 g,加入9 ml 6% NaOH和6 ml环氧丙烷,室温下反应48 h。反应结束后转移到含有3 ml 36%HCl的100 ml蒸馏水中,经沉淀、过滤即得羟丙基磺甲基化木质素(反应式见图1)。
图1
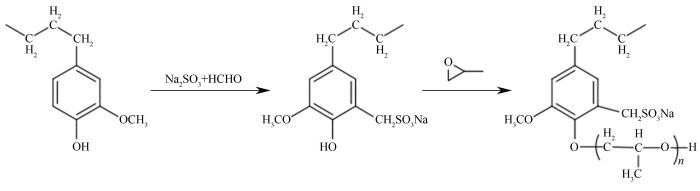
图1 改性木质素的制备流程
Fig.1 Preparation process of modified lignin
1.3 纤维素酶水解
取适量的微晶纤维素于Fritsch微型行星式高能球磨机中球磨2 h,转速为600 r/min,球磨机每运行5 min,休停10 min。
以球磨后微晶纤维素和添加了木质素的微晶纤维素为底物,木质素与微晶纤维素的添加量为0.53∶1,按酶用量30 FPU/g葡聚糖加入混合酶液。用pH为4.8的醋酸-醋酸钠缓冲液调节酶水解底物质量分数为5%。在50℃、180 r/min的条件下于恒温振荡器中反应72 h。采用美国Waters 1525分析型高效液相色谱检测水解液中各单糖的浓度,葡聚糖转化率按
式中,Y为葡聚糖转化率,%;c为水解液中葡萄糖浓度,g/L;v为水解总体系水解液体积,ml;0.9为葡萄糖转化系数;m为原料质量,g;w为原料中葡聚糖的含量,%。
1.4 木质素传感器的制备
以LiCl/DMSO为溶剂,溶解木质素,采用旋涂法将溶解后的木质素涂在金片表面。旋涂后的金片置于60℃的烘箱中干燥,待液膜变干后,用超纯水浸泡除去LiCl和DMSO。然后用氮气将膜的表面吹干,放入干燥器中备用。
1.5 分析方法
1.5.1 红外光谱分析
称取1 mg干燥后的木质素样品与100 mg的溴化钾混合,研磨成细粉末后进行压片,在Brucker VERTEX 80V红外光谱仪中进行检测。扫描范围为4000~400 cm-1,扫描分辨率为4 cm-1,扫描次数为60次/s。
1.5.2 核磁氢谱分析
分别取20 mg改性前后木质素样品,溶于0.5 ml DMSO-d6中,在25℃的条件下,使用Bruker Biospin公司的AVANCE III 600 MHz全数字化超导核磁共振谱仪在氢谱的模式下进行测试。测试条件:扫描次数16,数据采集时间2 s,扫描宽度12019 Hz,采集数据点65536。
1.5.3 XPS分析
利用岛津公司的AXIS UitraDLD X射线光电子能谱仪对木质素的表面元素和官能团组成进行分析。具体测试条件为:辐射源为Al Kα X光源,测试能量为1486.6 eV,测试管电压为15 kV,管电流为5 mA。
1.5.4 酚羟基测定
根据文献[17]采用Folin-Ciocalteu试剂法(FC法)进行酚羟基的测定。
(1)标准曲线绘制
精确称取一定量的香草醛,分别配制浓度为2.65、5.29、10.58、21.17、26.46、37.05 μmol/L的溶液50 ml,然后再加入3 ml FC试剂,充分摇匀30 s后加入10 ml 20% Na2CO3,搅拌反应2 h。利用TU-1900型紫外分光光度计在760 nm下测试浓液吸光度,得到标准曲线为
(2)木质素样品测定
称取10 mg待测样品,溶解于100 ml蒸馏水中(为保证木质素充分溶解,可加入少量的NaOH),按上述步骤测量吸光度并对照标准曲线计算酚羟基含量。
1.5.5 表面电荷测定
根据文献[18]测定改性前后木质素的表面电荷。将120 mg木质素溶解在10 g的0.1 mol/L NaOH溶液中,加入3 g的1 mol/L HCl,混合均匀。加入30 g 0.1 mol/L NaOH 进行中和,以不含木质素的空白为对照样,用0.1 mol/L HCl滴定样品和空白样品至pH为4.8。木质素样品溶液的滴定体积记为Vsample,空白样品的滴定体积记为Vblank,表面电荷Q的计算公式如下:
式中,M为HCl的浓度,0.1 mol/L;W为木质素样品的质量,0.12 g。
1.5.6 接触角测定
改性前后的木质素分别配制成质量分数为0.25%水溶液,可加入微量的NaOH保证木质素充分溶解。取100 μl的木质素溶液和羟丙基磺甲基化木质素溶液分别涂覆于载玻片上,室温下风干24 h,在105℃的烘箱中干燥1 h除去剩余的水分。使用瑞典百欧林公司的T200-Auto3 Plus光学接触测试仪进行接触角的测定。
1.5.7 QCM分析
将涂覆的木质素薄膜金片放入QCM模块中,温度设定为40℃,以0.1 ml/min的速度向模块中通入pH为4.8的醋酸-醋酸钠缓冲液。待基线稳定后,通入浓度为0.1 mg/ml的纤维素酶溶液,30 min后停止通入酶溶液,再次向模块中通入缓冲液,冲洗15 min。 每组实验至少测定3次,频率选用3次测定的平均值。所有频率变化的基频为5 MHz,频率为15、25、35和45 MHz的倍频被同时监测。数据处理时选用3倍频(15 MHz)下的数据。
2 结果与讨论
2.1 红外光谱分析
木质素和羟丙基磺甲基化木质素的红外光谱图如图2所示,主要峰的范围在4000~400 cm-1。3420 cm-1处的吸收峰为羟基的伸缩振动,2931 cm-1处为亚甲基、次甲基伸缩振动的吸收峰。1590、1509、1420 cm-1处的吸收峰为苯环骨架振动,说明改性后的木质素芳香环结构保存完好。与木质素相比,2931 cm-1处改性后木质素的吸收峰增强,表明木质素中甲基、亚甲基的含量增多。改性后木质素在1147、1070、532 cm-1处的吸收峰较强,该处为磺酸基团的特征峰[19-20],说明木质素的结构中引入了磺酸基团。
图2
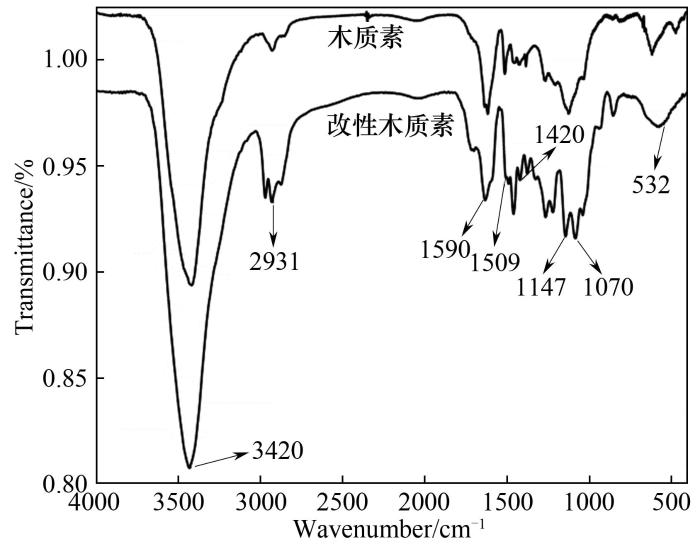
图2 改性木质素和木质素的红外光谱图
Fig.2 FT-IR spectra of modified lignin and original lignin
2.2 核磁氢谱分析
木质素改性前后的核磁氢谱图如图3所示。δ=3.10~3.32是酚羟基的质子峰[21],从图3中可明显看出,改性木质素在此处的信号强度与木质素相比有所减弱,说明经过改性后木质素中的酚羟基被封闭。此外,δ=3.32~4.00是—CH2SO3Na中亚甲基的质子峰,羟丙基磺甲基化改性后的木质素在此处的信号强度增加,表明改性后木质素的结构中成功接入了磺酸基团。
图3
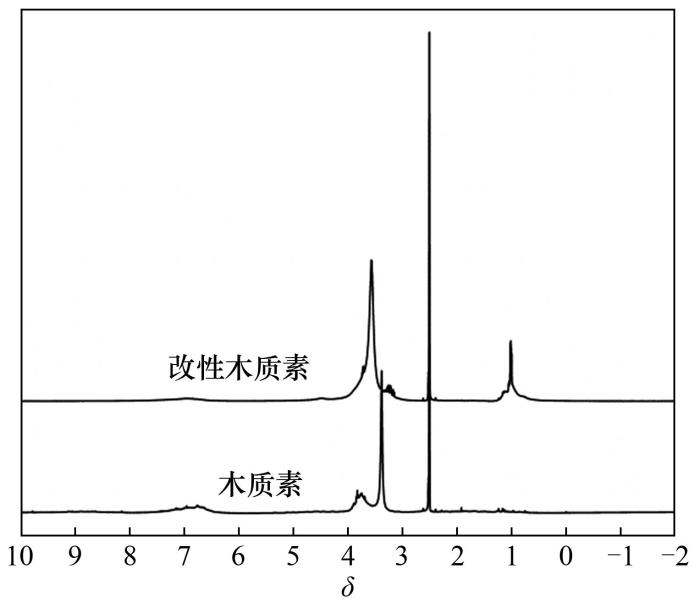
图3 改性木质素和木质素的核磁氢谱图
Fig.3 1H NMR spectra of modified lignin and original lignin
2.3 木质素表面特性分析
木质素和羟丙基磺甲基木质素的表面元素含量通过XPS进行测定,结果如表1所示。从表中可知,木质素未改性前的C元素含量为77.97%,O元素的含量为21.65%,S元素含量为0.38%。经过羟丙基磺甲基化改性后,木质素中C元素含量降低至77.33%,O元素的含量为21.89%,由于木质素结构中磺酸基团的引入,S元素的含量提升至0.78%。
表1 木质素和羟丙基磺甲基木质素的表面特性
Table 1
| 样品 | 元素组成/% | 酚羟基含量/(mmol/g) | 表面电荷/(mmol/g) | ||
|---|---|---|---|---|---|
| C | O | S | |||
| 木质素 | 77.97±0.03 | 21.65±0.01 | 0.38±0.02 | 5.28±0.21 | -0.33±0.04 |
| 羟丙基磺甲基木质素 | 77.33±0.03 | 21.89±0.02 | 0.78±0.05 | 0.36±0.01 | -0.58±0.02 |
新窗口打开| 下载CSV
木质素与改性木质素的酚羟基含量由FC法测得(表1),Xu等[22]已经运用这一方法对不同碱预处理甘蔗渣制备的木质素中酚羟基的含量进行测定与比较,并进一步探究其对酶水解的影响,FC法被认为是一种简单、快速地测定木质素酚羟基的方法[23]。根据表1可知,木质素中酚羟基的含量为5.28 mmol/g,羟丙基磺甲基木质素中酚羟基的含量为0.36 mmol/g,改性后木质素中的酚羟基含量远低于改性前木质素,意味着木质素中大量的酚羟基在经过羟丙基磺甲基化反应后得到成功封闭。
纤维素酶水解过程中,木质素和纤维素酶之间的吸附会受到疏水作用和静电作用的影响[24-25],例如,Yu等[26]发现在酶水解过程中添加阳离子聚合物能够通过静电吸引增强纤维素酶对纤维素的吸引,达到改善酶水解效果的目的。在研究纤维素酶对低共熔溶剂(deep eutectic solvent, DES)提取的木质素的非生产性吸附时,Song等[27]发现木质素在DES处理过程中会发生缩合,这些缩合的芳香结构通过疏水作用增加了对酶的吸附。因此本研究测定了木质素和改性木质素的疏水性和表面电荷。从表1中表面电荷的数据可以看出,木质素和羟丙基磺甲基木质素的表面电荷均具有负电性,分别为-0.33 mmol/g和-0.58 mmol/g,木质素经过改性后,在木质素结构中引入了磺酸基团,使得其负电性得到提高。木质素的疏水性则通过木质素的接触角来表征,图4为木质素改性前后的接触角,两种木质素接触角的大小为:改性前木质素>改性后木质素。与木质素相比,改性后的羟丙基磺甲基木质素的接触角减小,说明改性后的木质素疏水性减弱。经过改性,木质素的酚羟基含量降低,同时结构中引入了亲水性基团磺酸基,导致了改性后木质素负电性增强、疏水性减弱[28]。
图4

图4 木质素(a)和羟丙基磺甲基木质素(b)的接触角
Fig.4 The contact angle of lignin (a) and hydroxypropyl sulfonmethyl lignin (b)
2.4 木质素对纤维素酶的吸附
耗散型石英晶体微天平(QCM-D)是一种极其灵敏的质量传感器,目前已广泛应用于多种领域[29]。它利用石英晶体的压电效应,通过监测表面频率(∆F)的变化,了解传感器表面微质量的变化以及表面薄膜的性能[30]。本文借助QCM-D实时、原位地研究木质素对纤维素酶的吸附影响,纤维素酶在木质素、羟丙基磺甲基木质素薄膜上的吸附过程如图5所示。由图可知,纤维素酶在木质素薄膜上的吸附均分为两段:快速吸附(Ⅰ)和缓慢吸附(Ⅱ)。通入酶溶液后的前10 min为快速吸附阶段,之后的20 min为缓慢吸附阶段。在通入缓冲液后(Ⅲ),两种木质素薄膜吸附纤维素酶的频率均有所上升,由于QCM-D输出的频率与传感器上薄膜的质量成反比,说明木质素薄膜的质量在减少,仅有少量的纤维素酶被缓冲液冲洗掉。
图5
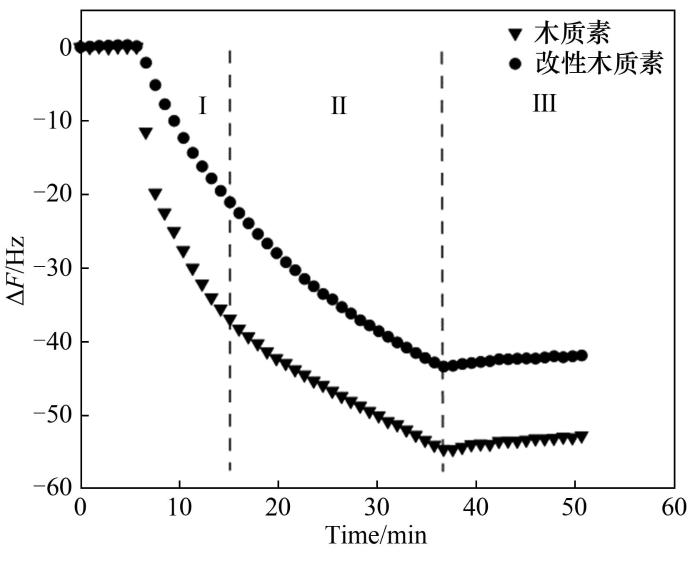
图5 纤维素酶在木质素薄膜上的吸附
Fig.5 Adsorption of cellulase on lignin film
通过对两种木质素的最大吸附频率的比较发现羟丙基磺甲基化木质素对纤维素酶的吸附量远低于原木质素,说明在酶水解过程中,与未改性木质素相比,经羟丙基磺甲基化的木质素与纤维素酶之间产生的无效吸附更少。纤维素酶是由内切葡聚糖酶EG、纤维二糖水解酶CBH、β-葡萄糖苷酶β-G三部分组成[31]。一般情况下,纤维素酶具有电荷,因此它们可以被木质素表面相反或相同的电荷吸附或排斥,有研究表明,CBHⅠ和EGⅠ在pH=4.8时带负电荷[32-33]。根据前面木质素的表面电荷可知,羟丙基磺甲基化木质素的负电性更高,几乎是改性前木质素的两倍,羟丙基磺甲基化木质素与纤维素酶之间会有更强的静电斥力,因此会减少木质素与纤维素酶之间的非生产吸附,有利于提高纤维素的酶水解效率。Li等[34]在研究不同分子量木质素对酶水解的影响时也发现,负电性更高的木质素对纤维素表现出较低的亲和力,说明木质素表面电荷的差异会导致纤维素酶与木质素亲和力的不同。除了静电作用外,木质素与纤维素酶之间的吸附也受到疏水作用的影响[35]。酶水解过程中,底物木质纤维素的疏水性会影响纤维素酶在底物上的吸附,木质素的存在则会增加底物的疏水性[36]。此外,木质素表面的疏水基团还会与纤维素酶结构中芳香性氨基酸的残基进行结合,导致木质素对纤维素酶的不可逆吸附[18]。Yu等[37]在研究糠醛残渣木质素对纤维素酶的非生产性吸附时发现,绿液与过氧化氢或乙醇预处理可通过增加木质素的亲水性来减少纤维素酶和β-葡萄糖苷酶在木质素上的吸附。Huang等[38]研究有机溶剂木质素对酶水解的抑制作用时发现,降低木质素的疏水性能减少木质素与酶的相互作用。同样地,本研究中也有类似的发现,结合改性前后木质素表面疏水性的大小可知,木质素经羟丙基磺甲基化改性后,由于木质素结构中酚羟基含量的减少,亲水性基团磺酸基的引入,改性后木质素表面的疏水性显著降低,导致木质素与纤维素酶之间的作用力减弱,发生的无效吸附也因此减少。
QCM获得的频率数据还可以进一步与指数衰减模型[
式中,ΔFmax为达到最大吸附量时的频率,Hz;t为时间,min;τ为吸附速率的倒数,min;Δm表示吸附质量,ng/cm2;c为质量敏感常数,这里取c=17.7 ng/(cm2·Hz);ΔF为频率,Hz;n为倍频值,n=3,5,7,9,11,这里取n=3。
表2是纤维素酶在木质素薄膜上的吸附参数,拟合相关系数R2均达到0.9以上。由表可知,两种木质素对纤维素酶的吸附能力具有明显的差异,羟丙基磺甲基化木质素的吸附速率1/τ低于未改性木质素,最大吸附量ΔF也较少,此外,根据表中的最大吸附量和不可逆吸附量可知,纤维素酶在羟丙基磺甲基化木质素薄膜上的解吸量更多,达到43.1 ng/cm2。表明羟丙基磺甲基化木质素高负电性、低疏水性的特点使得其与纤维素酶之间的吸附疏松,作用较弱,对纤维素酶的吸附能力较低。
表2 纤维素酶在木质素薄膜上的吸附参数
Table 2
| 样品 | ( | R2 | 最大吸附量/(ng/cm2) | 不可逆吸附量/(ng/cm2) | 解吸量/(ng/cm2) | |
|---|---|---|---|---|---|---|
| 木质素膜 | 57.81 | 0.064 | 0.92 | 341.1 | 311.9 | 29.2 |
| 羟丙基磺甲基木质素膜 | 50.59 | 0.053 | 0.95 | 298.5 | 255.4 | 43.1 |
新窗口打开| 下载CSV
纤维素酶在木质素薄膜上的吸附过程也可以用ΔD-ΔF的函数表示,这种表示方法消除了时间参数,能够直接比较ΔD和ΔF的比值。较低的
图6是纤维素酶在木质素薄膜吸附过程中ΔD、ΔF的变化。木质素和羟丙基磺甲基木质素薄膜的
图6
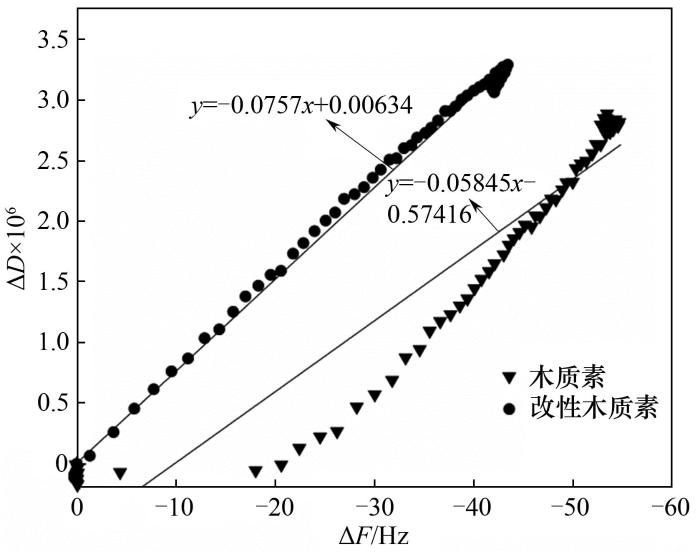
图6 纤维素酶在木质素薄膜吸附过程中ΔD随ΔF的变化
Fig.6 Change of dissipation (ΔD) versus frequency (ΔF) during the enzymatic adsorption of lignin films
2.5 木质素对纤维素酶水解的影响
以微晶纤维素(Avicel)和添加了木质素的微晶纤维素为底物,在酶用量30 FPU/g、pH为4.8的条件下进行水解,图7为酶水解72 h后葡聚糖的转化率。
图7
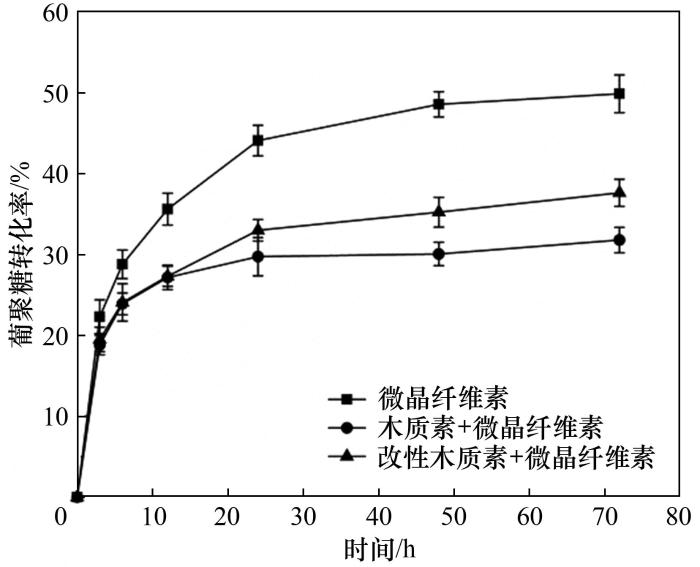
图7 木质素对酶水解效率的影响
Fig.7 Effects of lignin on enzymatic hydrolysis efficiency
根据图7可知,Avicel水解72 h后的葡聚糖转化率为49.91%。加入木质素后,由于木质素与纤维素酶之间有较强的非生产性吸附,对酶水解产生抑制作用,使得葡聚糖转化率降至31.81%。Li等[42]认为木质素对纤维素酶水解有抑制作用,通过减少纤维素酶对纤维素的可及性,降低酶水解效率。因此,木质素的存在不仅对酶有一定的吸附,还会阻碍纤维素与酶的接触机会。当加入羟丙基磺甲基化改性的木质素时,葡聚糖转化率为37.65%,与木质素相比提升了18.36%。Xu等[43]也在研究中发现,与酶解木质素相比,预处理后的甘蔗渣分离木质素具有较低的负Zeta电位、较高的酚羟基和疏水性,对纤维素酶具有较强的非生产性吸附能力。由此可以进一步证明,木质素经过羟丙基磺甲基化改性后,由于其高负电性、低疏水性的特点使其与纤维素酶之间的非生产性吸附减少,为纤维素酶与纤维素之间的接触提供了更多的机会,从而提高酶水解效率。
3 结论
经过羟丙基磺甲基化改性,木质素的酚羟基含量降低,同时结构中引入了亲水性基团磺酸基,导致了改性后木质素负电性增强、疏水性减弱。基于耗散型石英晶体微天平的动态参数可知,由于羟丙基磺甲基化木质素具有较高的表面负电性和较低的疏水性,使得纤维素酶与木质素之间的作用力减弱,对纤维素酶的吸附能力降低。将羟丙基磺甲基化木质素添加到微晶纤维素的水解体系中,纤维素酶水解72 h后,与未改性木质素相比,葡聚糖转化率提升了18.36%。说明改变木质素的表面特性,能够缓解木质素对酶水解的抑制作用,可进一步提高酶水解转化效率。
- 刚刚!2026年中科院分区,公布!本次看点:中科院分区变更为新锐分区;不再单独发布预警期刊;37种期刊“under review”~
- 这些重要报纸理论版都支持邮箱投稿!回复极快!
- GB/T 7714-2025与GB/T 7714-2015相比,变更了哪些,对期刊参考文献格式有什么影响?
- 别被这个老掉牙的报纸理论版投稿邮箱误导了!最新核实91个报纸理论版投稿邮箱通道,一次集齐
- 喜报!《中国博物馆》入选CSSCI扩展版来源期刊(最新CSSCI南大核心期刊目录2025-2026版)!新入选!
- 2025年中科院分区表已公布!Scientific Reports降至三区
- 国内核心期刊分级情况概览及说明!本篇适用人群:需要发南核、北核、CSCD、科核、AMI、SCD、RCCSE期刊的学者
- CSSCI官方早就公布了最新南核目录,有心的人已经拿到并且投入使用!附南核目录新增期刊!
- 北大核心期刊目录换届,我们应该熟知的10个知识点。
- 注意,最新期刊论文格式标准已发布,论文写作规则发生重大变化!文字版GB/T 7713.2—2022 学术论文编写规则

 0373-5939925
0373-5939925 2851259250@qq.com
2851259250@qq.com



